| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《物质的量》考点预测(2017年强化版)(六)
参考答案:B 本题解析:根据物质的化学式可知1mol的硫酸分子中含4NA个O原子,amolH2SO4中含有b个氧原子,则1:a=4NA:b,所以NA= b/4a /mol,因此选项是B。 本题难度:一般 4、选择题 下列各组物质中,所含分子数相同的是( ) |
参考答案:B
本题解析:只要物质的物质的量相等,则根据 可知,物质的分子数就是相等的。选项A中氢气的物质的量是5mol,氧气的物质的量是10/32mol;B中氨气的物质的量是0.25mol,CO2的物质的量也是0.25mol;C中水的物质的量是0.5mol;D中氢气的物质的量是0.01mol,所以正确的答案选B。
可知,物质的分子数就是相等的。选项A中氢气的物质的量是5mol,氧气的物质的量是10/32mol;B中氨气的物质的量是0.25mol,CO2的物质的量也是0.25mol;C中水的物质的量是0.5mol;D中氢气的物质的量是0.01mol,所以正确的答案选B。
本题难度:一般
5、选择题 将40克NaOH溶于水中,配制成1L溶液,则该溶液的物质的量浓度为
A.0.1mol/L
B.0.5mol/L
C.4mol/L
D.1mol/L
参考答案:D
本题解析:分析:根据溶质的质量计算溶质的物质的量,根据c= 计算溶液的物质的量浓度.
计算溶液的物质的量浓度.
解答:n(NaOH)=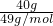 =1mol,
=1mol,
则c= =
= =1mol/L.
=1mol/L.
故选D.
点评:本题考查物质的量的有关计算,题目难度不大,注意物质的量与质量、浓度的计算公式的运用.
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《离子共存》高频考.. | |