��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����й�ʵ��ԭ���������ͽ��۶���ȷ����
[? ]
A.��FeCl3��Һ�еμӹ�����ˮ������ȡFe(OH)3����
B.ȡ������ҺX�������м����������ư�ˮ���ټӼ���KSCN��Һ����Һ��죬˵��X��Һ��һ������
Fe2+
C.���������������ӵĻ����Һ�м�������NaOH��Һ�������ú��Һ���ɳ�ȥ������������
D.��֪I3-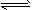 I2+I-����ʢ��KI3��Һ���Թ��м�������CCl4�����ú�CCl4������ɫ��˵��KI3��CCl4
I2+I-����ʢ��KI3��Һ���Թ��м�������CCl4�����ú�CCl4������ɫ��˵��KI3��CCl4
�е��ܽ�ȱ���ˮ�еĴ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ʵ���� ʵ�����ô���ʯ��ԭ����ȡ��ȫ����ɱ�����������ơ�����ʯ����Ҫ���������������������ᴿ����ʯ��ʵ�鲽�裺
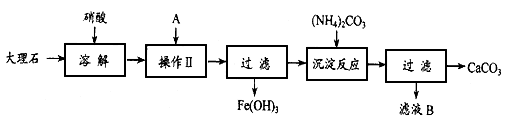
��1���ܽ����ʯʱ�����������ͬ�����ԭ����____________ ��
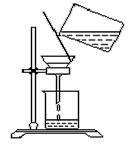
��2������ʱ��ijѧ���IJ�������ͼ����ָ��ͼ�еĴ�����_______________��
��3��������Һ���Ƿ�����ѡ�õ��Լ���________������________����Ӧ�����ӷ���ʽ��__________��
��4��д������̼�����������Ӧ�����ӷ���ʽ��_____________ ��
�ο��𰸣���1�����������ˮ
��2���������¶�û��(��Ӧ��)����(����)��ֽ�ϣ�©����û��(��Ӧ��)�����ձ��ڱڣ�
��3�����軯����Һ(��KSCN)����Һ��Ѫ��ɫ�� Fe3++3SCN-==Fe(SCN)3
��4��Ca2++CO32-==CaCO3��
���������
�����Ѷȣ�һ��
3��ʵ���� TiO2��Ϳ�ϡ��������ױƷ���������ż���㷺��Ӧ�á�ijѧϰС��ͬѧ��ʵ������������(��Ҫ�ɷ�ΪFeTiO3������SiO2������)ģ�ҵ����TiO2��?�����������
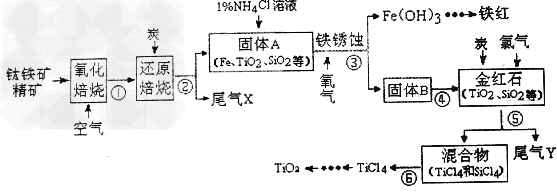
�ش��������⣺
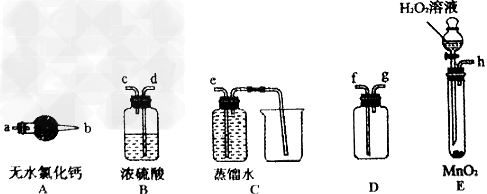
(1)ѡ���Ҫ��װ���Ʊ����ռ��������������������������װ�õ���ȷ����˳��Ϊ_________________?(�������ӿڵ���ĸ���)�����װ��E�����ԵIJ�������Ϊ___________��
(2)������������绯ѧ��ʴ�Ĺ����У�O2������缫��Ӧ�⣬����������һ����ѧ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_________________
(3)�������й���B����ϴ�ӵõ����ʯ����֤���ʯCl�C��ϴ����ʵ�鷽����____________
(4)������в�����β��Y�к�������Cl2����Ⱦ���������п���������Cl2���Լ�Ϊ_______(����ĸ���)?��
a������ʳ��ˮ?b��Ũ����?c��ŨNaOH��Һ?d��ʯ����
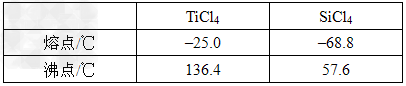
(5)�����±����ݣ�������з���TiCl4��SiCl4�����IJ�������Ϊ_______�����õ�����Ҫ�����������ƾ��ơ��¶ȼ����________________��
�ο��𰸣�(1)hdcfgab(��hdcfg��habfg)���õ�������h��������ĩ�˽���ʢˮ��ˮ���У��رշ�Һ©���Ļ��������������Թܣ������ܿ�������ð����������һ��ʱ���������ˮ�����γ�һ���ȶ���Һ����֤������������
(2)4Fe(OH)2?+?O2?+?2H2O?=?4Fe(OH)3
(3)ȥ���һ��ϴ��Һ������μ������ữ����������Һ���ް�ɫ�����γɣ�֤��Cl�C��ϴ��
(4)cd
(5)����������ƿ�������ܡ�ţ�ǹܡ���ƿ
���������
�����Ѷȣ�һ��
4��ѡ���� 1-������������Ũ���������£�ͨ��������Ӧ�Ƶ����ᶡ������Ӧ�¶�Ϊ115��125�棬��Ӧװ����ͼ�������й������������

[? ]
A��������ˮԡ����
B��������������֮һ����������
C���ᴿ���ᶡ��ֻҪ������������Һϴ�Ӻ�����ˮϴ�Ӽ����
D�������������������1-������ת����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ʵ���� ij�о���ѧϰС�����о���Fe2+�Ʊ�Fe(OH)2�Ĺ����У����������ʵ�鷽����
��ʵ����ơ�������������ͼ����ʵ�飬����A�еķ�Ӧ��ʼʱ�����ɼ�C���ڴ�״̬��һ��ʱ��رյ��ɼ�C������A�еķ�Ӧ���ڽ��С�

��1��������_______�����й۲쵽��ɫ��������ʵ�����漰���Ļ�ѧ����ʽ�У�____________________________ ��
��̽��˼����ʵ���������ʵ���г��ְ�ɫ�ij�������ת��Ϊ����ɫ����ɫ����ô��ν��ͳ��ֻ���ɫ����ɫ�������أ�
��2����ͬѧ�������Ϻõ�Fe(OH)2������Ϣ��?

�Ķ������Ϻ��������ʵ���г��ֻ���ɫ����ɫ������Ľ����ǣ�__________ ���������ἰ����ɫFe3(OH)8�������������ʽ��ʾ��д��__________________��
��3����ͬѧ������ɫԭ������ɫ����ɫ�����ܵ������ɫ�����ɫ�ij�ʶ����Ϊ��ɫ�������γ�Fe(OH)2��nH2O���¡�����ˮԡ�ķ�ʽ���ȡ�����һ�������ɵ���ɫ�������۲쵽�������̱�����ơ�����ʱ��������һ���е��ɼ�CӦ����___________������رա���״̬������A�еķ�Ӧ�봦��___________���ֹͣ����������״̬��д����ʵ����֧����ͬѧ�۵�Ļ�ѧ����ʽ_______________��
��4����ӭ��μӸ��о�С������ۣ������һ�����о���Fe2+�Ʊ�Fe(OH)2�Ĺ����У������ڶԳ����ɡ��ס��䡰�̡���������к������͵�ʵ�������˼·��___________________________________ ��
�ο��𰸣���1��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe(OH)2��+Na2SO4��H2SO4+2NaOH=Na2SO4��2H2O (�кͷ�Ӧ����ʽ��д���۷�)
��2������Fe(OH)2���ֱ�����������������Fe(OH)3��FeO��Fe2O3��4H2O
��3����������Fe��OH��2��nH2O= Fe��OH��2+ nH2O
��4����Fe2+��Fe3+�Ļ��Һ�м���NaOH��Һ�۲����ɵij�������ɫ�Ƿ�Ϊ����ɫ�����߿��Խ�Fe(OH)3��Fe(OH)2��Ϻ�۲�����ɫ����
���������
�����Ѷȣ�һ��