微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。
若用下图所法实验装置可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
①a电极材料为_______,其电极反应式为_______________。
②电解液d可以是_______,则白色沉淀在电极上生成;也可以是_______,则白色沉淀在两极之间的溶液中生成。
A.纯水
B.NaCl 溶液
C.NaOH溶液
D.CuCl2溶液
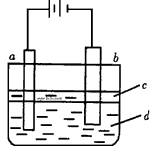
③液体c为苯,其作用是______________,在加入苯之前,对d溶液进行加热处理的目的是___________。
④为了在短时间内看到白色沉淀,可以采取的措施是____________________。
A.改用稀硫酸做电解液
B.适当增大电源电压
C.适当缩小两电极间距离
D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为 ___________。
2、实验题 晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl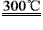 SiHCl3+H2
SiHCl3+H2
③SiHCl3与过量H2在1000~1100℃反应制得纯硅已知SiHCl3,能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为_________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点--84.7℃),提纯SiHCl3采用的方法为___________。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
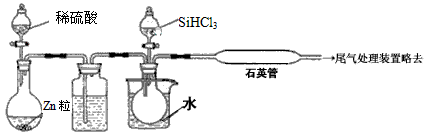
①装置B中的试剂是___________。装置C中的烧瓶需要加热,其目的是___________。
②反应一段时间后,装置D中观察到的现象是______________________,装置D不能采用普通玻璃管的原因是___________,装置D中发生反应的化学方程式为______________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及________。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂
(填写字母代号)是_________。
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液
3、实验题 实验室可用如图所示装置制取NaClO3。图中:a为氯气发生装 置.b为NaClO3的制备装置;c为尾气吸收装置。请回答下列问题。

(1)制取氯气的化学反应方程式(未配平)为:KMnO4+HCl(浓)→ MnCl2+KCl+Cl2↑+H2O,请将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目。? □+□
(2)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以滴下,经检查分液漏斗活塞没有堵塞,你认为应采取的措施是__________。实验时为了除去氯气中的氯化氢气体,可在a与b之间安装盛有_________(填写下列字母编号)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(3)装置b中发生反应的化学方程式为3Cl2 +6NaOH 5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________
5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________
(4)工业上用石灰乳代替烧碱溶液吸收尾气的原因是__________。工业上用60℃的Na2CO3溶液吸收 Cl2也可制得NaClO3,该反应的离子方程式为_____________ 。
4、选择题 下图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是

[? ]
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再冰醋酸
B.试管b中导气管下端管口不能浸入液面的目的是防止实验过程中产生倒吸现象
C.实验时加入试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动
D.试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇
5、实验题 “酒是陈的香”的原因之一是储存过程中生成了有香味的酯。实验室用下图所示装置制取乙酸乙酯。
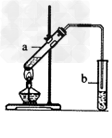
(1)试管a中生成乙酸乙酯的化学反应方程式是? 。
(2)试管b中盛放的试剂是? 溶液,试管b中的导管不伸入液面下的原因是? 。试管b中发生反应的化学方程式是? 。
(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有( 填序号)? 。
①单位时间里,生成1mol 乙酸乙酯,同时生成1mol 水
②单位时间里,生成1mol 乙酸乙酯,同时生成1mol 乙酸
③单位时间里,消耗1mol 乙醇,同时消耗1mol 乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化