微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 25℃时,浓度为0.1mol/L的某一元强碱MOH溶液与相同体积的某一元酸HA溶液混合后恰好呈中性。下列判断一定正确的是?(?)
A.HA酸溶液的pH值一定等于1
B.HA酸溶液的物质的量浓度一定等于0.1mol/L
C.中和后溶液中M+离子浓度一定等于A-离子浓度
D.中和后生成的盐MA一定没有发生水解
参考答案:C
本题解析:因酸碱都是一元的,所以恰好完全反应。由于酸HA的强弱不明确,要具体分析。若HA是强酸,则c=0.1mol/L,pH=1,此时A、B正确;若HA是弱酸,则c>0.1mol/L,MA水解。但,无论HA是强酸还是弱酸,溶液中的电荷恒等式c(H+)+c(M+)=c(OH-)+c(A-)总是成立的。
本题难度:一般
2、选择题 判断溶液为中性的依据是
A.c(OH-)=1×10-7 mol/L
B.c(H+)=1×10-7 mol/L
C.c(OH-)=c(H+)
D.pH=7
参考答案:C
本题解析:略
本题难度:简单
3、选择题 实验测得在常温下0.1mol・L-1某一元碱(BOH)pH≠13,0.1 mol・L-1的某一元酸(HA)溶液中,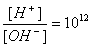 ,将两种溶液等体积混合后,溶液中离子浓度关系正确的是
,将两种溶液等体积混合后,溶液中离子浓度关系正确的是
A.C(A-)>C(B+)>C(H+)>C(OH-) ? B.C(B+)>C(A-)>C(H+)>C(OH-)
C.C(B+)>C(A-)>C(OH-)=C(H+) ? D.C(A-)>C(B+)>C(OH-) >C(H+)
参考答案:A
本题解析:在常温下0.1mol・L-1某一元碱(BOH)pH≠13,什么该碱不是强碱。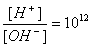 ,所以根据水的离子积常数可计算出氢离子浓度为0.1mol/,所以酸是强酸。二者等体积混合,恰好反应生成强酸弱碱盐BA,B+水解显酸性,所以选项A是正确的,答案选A。
,所以根据水的离子积常数可计算出氢离子浓度为0.1mol/,所以酸是强酸。二者等体积混合,恰好反应生成强酸弱碱盐BA,B+水解显酸性,所以选项A是正确的,答案选A。
本题难度:一般
4、选择题 在某温度时,测得纯水中的c(H+)=2.0×10-7 mol・L-1,则c( OH-)为
OH-)为
A.2.0×10-7 mol・L-1
B.0.1×10-7 mol・L-1
C.1.0×10-14/2.0×10-7 mol・L-1
D.无法确定
参考答案:A
本题解析:略
本题难度:简单
5、选择题 下图是向25.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH变化的图象,根据图象分析,下列结论中不正确的是?
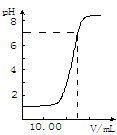
A.盐酸起始浓度为0.10 mol・L-1
B.NaOH溶液浓度为0.10 mol・L-1
C.滴到中点时,耗NaOH物质的量为0.0025mol
D.滴入碱量为20.00mL时,向混合溶液中滴入2滴酚酞试液,溶液显红色
参考答案:D
本题解析:D项:碱量为20.00mL时,溶液还呈酸性,故不显红色,故错。故选D。
点评:本题考查的是中和滴定时溶液的PH计算,指示剂的显色范围。难度中。注重对教材知识的学习。
本题难度:一般