微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在密闭容器中发生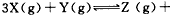 2W(g)反应,现在控制下列3种不同的条件:
2W(g)反应,现在控制下列3种不同的条件:
①400℃时,9 mol X与3 mol Y反应,
②400℃时,15 mol X与5 mol Y反应,
③300℃时,9 mol X与3 mol Y反应,
那么,反应开始时,正反应速率最大的是(填序号,下 同)_______,正反应速率最小的是_________
参考答案:②;③
本题解析:
本题难度:一般
2、选择题 下列说法错误的是( )
A.对于反应C(s)+CO2?(g)=2CO(g)△H>0,升高温度会加快化学反应速率
B.将n?mol?H2(g)、n?mol?I2(g)和2n?mol?H2?(g)、2n?mol?I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者
C.合成氨反应中,当3v(NH3)正=2v(H2)逆时,反应达到平衡
D.对于反应PCl5(g)?PCl3(g)+Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小
参考答案:A.升高温度,加快反应速率,与反应吸热与放热无关,故A正确;
B.由H2(g)+I2(g)?2HI(g)及恒温恒容的容器,前者与后者为等效平衡,所以平衡时H2的转化率相同,故B错误;
C.同种物质的正逆反应速率相等时,反应达到平衡状态,合成氨反应中,当3v(NH3)正=2v(H2)正=2v(H2)逆时,所以反应达到平衡,故C正确;
D.保持温度容积不变,又加入一定量的PCl5,反应物的浓度增大,平衡正向移动,但正向移动的趋势不大,PCl5的总量比原来的大,所以平衡时PCl5的转化率减小,故D正确;
故选B.
本题解析:
本题难度:一般
3、填空题 在硫酸工业中,通过下列反应使SO2转化为SO3:2SO2+O2 2SO3,ΔH<0,已知常压下平衡混合气体中SO3体积分数为91%。试回答:
2SO3,ΔH<0,已知常压下平衡混合气体中SO3体积分数为91%。试回答:
参考答案:
本题解析:
本题难度:一般
4、选择题 下图是可逆反应A+2B  ?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断

A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.D可能是气体.
D.A、B、C、D均为气体
参考答案:B
本题解析:由图像可知,降温后V正>V逆,平衡正向移动,所以正反应是一个放热反应,A错误;加压后V正>V逆,所以平衡正向移动,所以反应物气体系数大于生成物气体系数,所以D一定不可能是气体,所以选B。
本题难度:一般
5、选择题 以下反应均在密闭容器中进行,根据相应的图象,下列相关说法正确的是( )
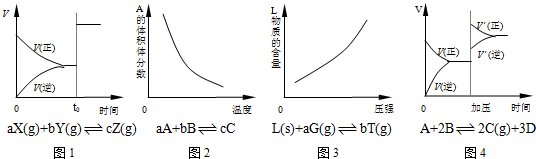
A.图1所示为t0时改变某一条件时速率变化,则改变的条件一定是加入催化剂
B.图2所示为反应达到平衡时温度对化学平衡的影响,则正反应为放热反应
C.图3所示为反应达到平衡时压强对化学平衡的影响,则反应方程式中a<b
D.图4所示为平衡后加压时反应速率的变化,则A、B是气体、D为固体或液体
参考答案:A.图1在t0时正逆反应速率都增大,平衡不移动,不一定是催化剂的原因,如a+b=c,增大压强,反应速率增大,平衡不移动,故A错误;
B.图2A的体积分数随温度的升高而降低,说明温度升高,平衡向正反应方向移动,则正反应为吸热反应,故B错误;
C.图3L物质的含量随压强的增大而增大,说明增大压强平衡向逆反应方向移动,则反应方程式中a<b,故C正确;
D.图4增大压强,平衡向正反应方向移动,说明气体反应物的化学计量数之和大于其它气体生成物的化学计量数之和,则则A、B是气体、D为固体或液体,故D正确.
故选CD.
本题解析:
本题难度:简单