|
高中化学知识点总结《影响化学反应速率的因素》高频考点特训(2017年练习版)(六)
2017-07-10 19:57:53
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率但不影响生成H2的总量,可向盐酸中加入适量的
[? ]
A.CaCO3(s)
B.Na2SO4溶液
C.KNO3溶液
D.CuSO4(s)
参考答案:B
本题解析:
本题难度:一般
2、选择题 能使碳酸钙的分解速率显著增大的措施是
A.升高温度
B.增加少量的CaCO3固体
C.加入MnO2
D.增大压强
|
参考答案:A
本题解析:A.使碳酸钙的分解速率显著增大,应升高温度;B.而碳酸钙为固体,则增加少量的CaCO3固体,反应物浓度不变,反应速率不变;C.该反应无需加入催化剂;D.增大压强,逆反应速率增大,但正反应速率不变,不能使分解速率增大;选A.
考点:考查影响化学反应速率的因素。
本题难度:一般
3、选择题 反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( ) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入H2O(g)使体系压强增大
D.保持压强不变,充入N2使容器体积变大
参考答案:A
本题解析:C(碳)为固态反应物,增加其用量对反应速率几乎没有影响,A项符合题意;容器体积缩小一半相当于压强增大一倍,浓度增大,反应速率增大,B项不符合;充入H2O(g),体积不变,反应速率加快,C项不符合;压强不变,充入N2,体积增大,气体的浓度变小,反应速率减小,D项不符合。
本题难度:一般
4、选择题 下列措施对增大反应速率明显有效的是
[? ]
A.Na与水反应时增大水的用量
B.Fe与稀硫酸反应制取氢气时,改用浓硫酸
C.在K2SO4与BaCl2两溶液反应时,增大压强
D.将铝片改为铝粉,做铝与氧气反应的实验
参考答案:D
本题解析:
本题难度:一般
5、计算题 在一个容积不变的反应器中,要求调节体系的温度使下列反应达到平衡时,保持容器内气体的总物质的量为12 mol。
已知反应A(g)+2B(g) 2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。 2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。
(1)若x=5.5时,需要降低体系的温度使反应在平衡时达到题设条件,则正反应为_______(填“吸热”或“放热”)反应。
(2)欲使起始反应维持向逆反应方向进行,则x的取值范围为_________。
(3)在一定温度下的上述平衡体系中,另按1∶2 的物质的量之比通入D和E两种气体(此时容器内气体的总物质的量不要求保持12 mol),按下式反应:D(g)+E(g) 2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。 2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。
参考答案:(1)放热(2)2.5<x<3.5
(3)2m+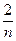
本题解析:(1)? A(g)? +? 2B(g) 2C(g) 2C(g)
起始/mol? 6.5? x?2
平衡n总="12" mol
当x=5.5时,6.5+5.5+2=13>12,降温使平衡向右移动,使n总="12" mol,故正反应为放热反应。
(2)若维持反应向逆反应方向进行,则有:
6.5+x+2<12,所以x<3.5。
设C转化了a? mol则:
A(g)? +? 2B(g) 2C(g) 2C(g)
起始6.5? x? 2
平衡6.5+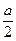 ? x+a? 2-a ? x+a? 2-a
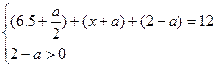
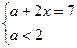 ?所以x>2.5 ?所以x>2.5
故x的取值范围是2.5<x<3.5。
(3)另有反应:D(g)? +? E(g) 2F(g) 2F(g)
起始:? m? n(E)? n
新平衡:(m+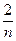 )∶[n(E)+ )∶[n(E)+ 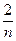 ]=1∶2。 ]=1∶2。
由于是等体积反应,保持(m+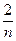 )∶[n(E)+ )∶[n(E)+ 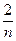 ]=1∶2即可,n(E)=2m+ ]=1∶2即可,n(E)=2m+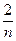 。 。
本题难度:简单
|