微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关沉淀溶解平衡的说法中,正确的是( )
A.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大
B.在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动
C.可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小
D.25℃时,KSP(AgCl)>KSP(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成
参考答案:A.因难溶盐电解质的Ksp与温度有关,不受其他因素的影响,所以加入蒸馏水,氯化银的KSP不变,故A错误;
B.碳酸根离子与酸反应生成二氧化碳和水,生成物的浓度减小,碳酸钙的沉淀溶解平衡正向移动,故B错误;
C.比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,故C错误;
D.KSP(AgCl)>KSP(AgI),沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色,故D正确;
故选:D.
本题解析:
本题难度:一般
2、选择题 常温下,CaSO4?在水中的沉淀溶解平衡曲线如图所示,已知 Ksp(CaSO4)=9×10-6。下列说法正确的是(?)

A.a点对应的KSP小于c点对应的KSP
B.a点变为b点将有沉淀生成
C.加入蒸馏水可以使c点变为d点
D.含有大量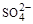 的溶液中肯定不存在Ca2+
的溶液中肯定不存在Ca2+
参考答案:B
本题解析:A、Ksp是一常数,温度不变Ksp不变,在曲线上的任意一点Ksp都相等,故A错误;
B、硫酸钙溶液中存在着溶解平衡,a点在平衡曲线上增大c(SO42-),平衡左移,将有沉淀生成,故B正确;
C、d点时溶液不饱和,蒸发溶剂水,c(SO42-)、c(Ba2+)均增大,故C错误;
D、硫酸钙溶液中存在着溶解平衡, SO42-、Ba2+溶液中都有,故D错误。
故选B。
点评:本题考查沉淀溶解平衡,题目难度中等,注意理解难溶电解质在水中的沉淀溶解平衡特点,正确理解和掌握溶度积KSP的概念。
本题难度:一般
3、选择题 下列说法正确的是( )
A.升高温度,AgCl的溶解度增大,Ksp不变
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
C.向AgCl饱和溶液中加入NaCl固体,AgCl的溶解度和Ksp都不变
D.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
参考答案:A、Ksp与温度有关,所以升高温度,AgCl的溶解度增大,Ksp也增大,故A错误;
B、物质的溶解度不一定随温度的升高而增大,如氢氧化钙溶液随温度的升高溶解度减小,故B错误;
C、氯化银饱和溶液中存在沉淀溶解平衡,向AgCl饱和溶液中加入NaCl固体,则平衡向生成沉淀的方向进行,氯化银的溶解度减小,Ksp只随温度的变化而变化,所以Ksp不变,故C错误;
D、氯化银饱和溶液中存在沉淀溶解平衡,氯离子浓度增大,平衡向生成沉淀方向进行,所以用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是(?)
A.AgCl的溶解度增大
B.AgCl的溶解度、Ksp均不变
C.Ksp(AgCl)增大
D.AgCl的溶解度、Ksp均增大
参考答案:B
本题解析: AgCl的溶解度、Ksp均与温度有关,温度不变则不变。故选B。
点评:本题考查的是溶解平衡的应用和溶解度的相关知识,题目难度不大,注意对基础知识的学习、掌握及应用。
本题难度:一般
5、填空题 (1)已知可逆反应:M(g)+N(g)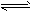 P(g)+Q(g) △H>0,请回答下列问题。
P(g)+Q(g) △H>0,请回答下列问题。
①若要增大M的转化率,在其他条件不变的情况下可以采取的措施为______(填序号)。
A.加入一定量M B.降低反应温度 C.升高反应温度
D.缩小容器体积 E.加入催化剂 F.分离出一定量P
②在某温度下起始反应物的浓度分别为:c(M)=1 mol/L,c(N)=2.4 mol/L,达到平衡后,M的转化率为
60%,此时N的转化率为_________;若保持温度不变,起始反应物的浓度改为:c(M)= 4 mol/L,c(N)=
a mol/L,达到平衡后,c(P)=2 mol/L,则a=__________mol/L。
(2)盖斯定律在生产和科学研究中有很重要的意义。试根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H来源:91考试网 www.91eXam.org=-24.8 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5 kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_____________________。
(3)一定温度下,向Na2CO3溶液中加入BaCl2和K2SO4,当两种沉淀共存时,c(CO32-):c(SO42-)=____。 [已知Ksp(BaSO4)=1.3×10-10,Ksp(BaCO3)=2.6×10-9]
参考答案:(1)①CF;②25%;6
(2)CO(g)+FeO(s)=Fe(s)+CO2(g) △H=-218.0kJ/mol
(3)20
本题解析:
本题难度:一般