微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 向盛有1mL0.1mol/LMgCl2溶液的试管中滴加1~2滴2mol/LNaOH溶液,观察到有白色沉淀生成,该反应的离子方程式是______.再滴加2滴0.1mol/LFeCl3溶液,观察到白色沉淀转化为红褐色沉淀,该反应的离子方程式是______.由以上现象可以推知,相同条件下Mg(OH)2和Fe(OH)3中溶解度较大的是______.
2、填空题 钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。已知:
SrSO4(s)  Sr2+(aq)+SO42-(aq) Ksp=2.5×10-7
Sr2+(aq)+SO42-(aq) Ksp=2.5×10-7
SrCO3(s)  Sr2+(aq)+CO32-(aq) Ksp=2.5×10-9
Sr2+(aq)+CO32-(aq) Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为________________________,该反应的平衡常数表达式为____________;该反应能发生的原因是___________________________________________。(用沉淀溶解平衡的有关理论解释)
(2)对于上述反应,实验证明增大CO32-的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将________;
②增大CO32-的浓度,平衡常数K将________。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。
实验所用的试剂为________;实验现象及其相应结论为____________________________。
3、选择题 向5mLNaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀谈黄色,再滴入滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系 ( )
A.AgCl=AgI=Ag2S
B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2 S
D.AgI>AgCl>Ag2S
4、选择题 某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水
②20 mL 0.5 mol・L-1的Na2SO4溶液
③40 mL 0.2 mol・L-1的Ba(OH)2溶液
④40 mL 0.1 mol・L-1的H2SO4溶液中,溶解至饱和
以上各溶液中,c(Ba2+)的大小顺序正确的是( )
A.③>①>④>②
B.③>①>②>④
C.①>④>③>②
D.①>③>④>②
5、选择题 下列说法正确的是(? )
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大
B.在一定温度下AgCl的水溶液中,Ag+和Cl-物质的量浓度的乘积是一个常数
C.25oC时Ksp(AgCl)=l.8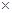 10-10,Ksp(AgI)=1.0×10-16,因此AgCl可以转化为AgI
10-10,Ksp(AgI)=1.0×10-16,因此AgCl可以转化为AgI
D.温度一定时,当溶液中Ag+和Cl-物质的量浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液