微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
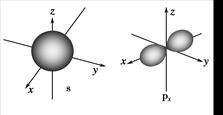
1、填空题 如图是s能级和p能级的原子轨道图,试回答问题:
 ?
?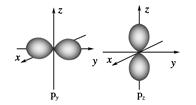
(1)s电子的原子轨道呈________形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是______电子,其电子云在空间有______________方向;元素X的名称是______,它的氢化物的电子式是________________________________________________________________________。
参考答案:(1) 球 1 纺锤 3? (2) 2p 三个互相垂直的伸展 氮?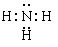
本题解析:(1)s电子的原子轨道呈球形,每个s能级有1个原子轨道;p电子的原子轨道呈纺锤形,每个p能级有3个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,则n=2,所以该元素的原子序数是7,是氮元素。其中原子中能量最高的是2p电子,其电子云在空间有三个互相垂直的伸展方向。其氢化物是氨气,含有极性键,其电子式是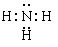 。
。
点评:该题是常识性知识的考查,难度不大。熟练记住核外电子的排布以及常见电子云的形成,并能灵活运用即可。
本题难度:一般
2、选择题 下列有关物质性质的描述不符合事实的是
A.有机物不导电
B.钠和钾的合金可做原子反应堆的导热剂
C.金刚石是自然界最硬的物质
D.过氧化钠可以作供氧剂
参考答案:A
本题解析:略
本题难度:一般
3、选择题 微量元素硒(Se)对人体有保健作用,我国鄂西地区含有丰富的硒矿资源.已知硒与氧同主族,与钾同周期,下列有关硒元素的性质描述错误的是( )
A.硒的氢化物以H2Se形式存在
B.硒的氧化物以Se2O3形式存在
C.硒的氢化物的热稳定性比硫化氢差
D.硒的最高价氧化物的水化物的化学式是H2SeO4
参考答案:B
本题解析:
本题难度:简单
4、填空题 (4分)(1)下列7种物质:
①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦干冰
固态时都为晶体,其中既有范德华力,又有非极性键的晶体是
(填写序号,下同),只存在离子键的是 ,熔化时只破坏
共价键的是 。
(2)下图是XeF4的结构示意图,据此判断XeF4是 (填“极性”、“非极性”)分子。

参考答案:(1)①⑤②(2)非极性(每空1分)
本题解析:(1)白磷形成的晶体是分子晶体,分子中含有范德华力与非极性键;水晶是二氧化硅,属于原子晶体,熔化破坏的是共价键;氯化铵、氢氧化钙、氟化钠、过氧化钠均是离子晶体,其中氯化铵、氢氧化钙、过氧化钠中既有离子键,又有共价键,而氟化钠中只有离子键;干冰是CO2形成的是分子晶体,含有极性键和范德华力。
(2)根据结构示意图可知,分子中正负电荷重心重合,属于非极性分子。
本题难度:一般
5、选择题 PtCl4・2NH3水溶液不导电加入AgNO3无现象加强碱无NH3放出下列说法正确的是(?)
A.配合物中中心原子的电荷数和配位数均为6
B.该配合物可能是平面正方形结构
C.Cl-和NH3分子均与Pt4+配位
D.配合物中Cl-与Pt4+配位,而NH3分子与Pt4+不配位
参考答案:C
本题解析:配合物中心原子的电荷数为+4,A错。由于配位键有两种形式:Pt-Cl和Pt-N,总共两类六条键,且这两种键的键长不相等,故不可能是平面正方形。实际上应该是八面体型,四个氯离子构成正方形,而两个氨分子在其上和下。B错。Pt4+分别以配位键与四个氯离子,两个氨分子中的氮原子成键。C对,D错。
点评:对配合物理论及形成配位键要了解清楚,本题难度不大。
本题难度:一般