微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设氯原子的质量为a g,12C原子的质量为b g,用Na表示阿伏加德罗常数的值,则下列说法正确的是(? )
①氯元素的相对原子质量为 ?②m g该氯原子的物质的量为
?②m g该氯原子的物质的量为 mol?③该氯原子的摩尔质量是aNa g?④n g该氯原子所含的电子数是
mol?③该氯原子的摩尔质量是aNa g?④n g该氯原子所含的电子数是
A.①②
B.③④
C.①③
D.②④
参考答案:D
本题解析:①中, 为该氯原子相对原子质量,而不是氯元素的相对原子质量。②中,m g氯原子中含
为该氯原子相对原子质量,而不是氯元素的相对原子质量。②中,m g氯原子中含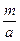 个氯原子,物质的量应为
个氯原子,物质的量应为 mol。③中氯原子的摩尔质量单位为g・mol-1。④中n g氯原子所含氯原子个数为
mol。③中氯原子的摩尔质量单位为g・mol-1。④中n g氯原子所含氯原子个数为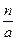 ,电子数为
,电子数为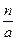 ×17。
×17。
本题难度:简单
2、选择题 下列叙述正确的是(?)。
A.1 mol H2O的质量为18 g/mol
B.CH4的摩尔质量为16 g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4 L
参考答案:C
本题解析:质量的单位是g,摩尔质量是g/mol,所以A、B都不正确。根据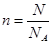 可知,3.01×1023个SO2分子是0.5mol,其质量是0.5mol×64g/mol=32g,C正确。气体摩尔体积只能适用于气体,所以D不正确,答案选C。
可知,3.01×1023个SO2分子是0.5mol,其质量是0.5mol×64g/mol=32g,C正确。气体摩尔体积只能适用于气体,所以D不正确,答案选C。
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA
B.标准状况下,由H2O2制得4.48LO2转移的电子数目为0.8NA
C.14 g 由乙烯与环丙烷组成的混合气体含有的碳原子数目为NA
D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA
参考答案:C
本题解析:A、标况下苯为液体,不能用气体摩尔体积计算,错误;B、氧元素有-1价到0价,生成0.2mol氧气,转移电子为0.4mol,错误;C、乙烯和环丙烷的最简式均为CH2,式量为14,故碳原子数为为NA,正确;D、该溶液中含有H+数目为0.01×1=0.01mol,错误。
本题难度:一般
4、计算题 已知氯元素的近似平均相对原子质量为35.5,由 、
、 和
和 构成的11.7g氯化钠晶体中含
构成的11.7g氯化钠晶体中含 的质量是多少?11.7g该晶体刚好能和某200mL的AgNO3溶液完全反应,则该AgNO3溶液的物质的量浓度是多少?
的质量是多少?11.7g该晶体刚好能和某200mL的AgNO3溶液完全反应,则该AgNO3溶液的物质的量浓度是多少?
参考答案:
解:n(NaCl)=0.2mol ,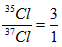
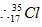 为0.15mol,质量为0.15mol×35g/mol=5.25g
为0.15mol,质量为0.15mol×35g/mol=5.25g
NaCl ~ AgCl
58.5 1mol
11.7g 0.2L×C(AgNO3)
C(AgNO3)=1mol/L
答: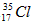 的质量为5.25g;硝酸银溶液的物质的量浓度为1mol/L。
的质量为5.25g;硝酸银溶液的物质的量浓度为1mol/L。
本题解析:
本题难度:一般
5、选择题 用等体积的0.1 mol?L-1 BaCl2溶液,分别使相同体积的Fe2 (SO4 )3、Na2SO4、KAl(SO4)2三种溶液中的SO42-恰好完全沉淀,则三种硫酸盐溶液的物质的量浓度之比为
A.3∶2∶3
B.3∶1∶2
C.2∶6∶3
D.1∶1∶1
参考答案:C
本题解析:根据题意知,等体积的0.1mol/L的BaCl2溶液,可使相同体积的三种溶液的SO42-完全沉淀,则Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中n(SO42-)相同,根据硫酸根守恒可知,3n[Fe2(SO4)3]= n(SO42-),n(Na2SO4)=n(SO42-),2n[KAl(SO4)2]= n(SO42-),三种溶液的体积相同,物质的量浓度之比等于溶质物质的量之比,所以三种硫酸盐的物质的量浓度之比为c[Fe2(SO4)3]:c(Na2SO4):c[KAl(SO4)2]= 2:6:3,选C。
本题难度:一般