��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��25 ml 0.1 mol �� L-1NaOH��Һ����μ���0.2mol �� L-1CH3COOH��Һ����ҺpH�仯������ͼ��ʾ�������й�����Ũ�ȵıȽ���ȷ����
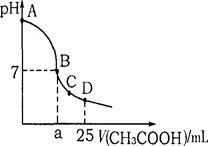
A����A��B����һ��(����A��B��)����Һ�п�����c (Na+) > c (CH3COO��) >c (OH��) > c (H+)
B����B�㣬a>12.5������c (Na+) ="c" (CH3COO��) =" c" (OH��)=" c" (H+)
C����C�㣬c (CH3COO��) > c (Na+) > c (OH��) > c (H+)
D����D�㣬c (CH3COO��) +c (CH3COOH) =" c" (Na+)
�ο��𰸣�A
�����������B��PH=7��������������c (Na+) +c (H+)="c" (CH3COO��) + c (OH��)����C�㣬c (CH3COO��) > c (Na+)? > c (H+)> c (OH��)����D�㣬c (CH3COO��) +c (CH3COOH) =" 2c" (Na+)
�����Ѷȣ�һ��
2������� ��10�֣���1�������ͬ��Ũ�Ⱦ�Ϊ0��2mol/L������ʹ�����Һ�ֱ��ˮϡ��10������Һ��pH�ֱ���m��n����m��n�Ĺ�ϵ��________��ϡ�ͺ�����Һ�к�NaOH������_______��
��2��25��ʱ��pH=3�Ĵ�����Һ��pH=11������������Һ�������ϣ���Ϻ���Һ��_____������ԡ������ԡ������ԡ�������Ϻ���Һ������Ũ���ɴ�С��˳����_______________________��
��3��25��ʱ����VamLpH=1��������Һ��VbmLpH=12������������Һ���ǡ�ó����ԣ���Va��Vb=________��
�ο��𰸣���1��m��n?��ͬ?��2������?c��CH3COO������c��Na������c��H������c��OH����?��3��1�U10
�����������1�����������ᣬϡ�������ڵ��룬��ϡ�ͺ�Ĵ���������Ũ����Ȼ��ͬ���������Ի��������ǿ�ڴ���ģ���pHС�ڴ���ġ�����Ũ�Ⱥ��������ͬ�������к��������Ƶ���������ͬ�ġ�
��2�����������ᣬ����pH=3�Ĵ�����Һ��pH=11������������Һ�������Ϻ����ǹ����ģ������Һ�����ԡ����Ի�Ϻ���Һ������Ũ���ɴ�С��˳����c��CH3COO������c��Na������c��H������c��OH������
��3��ǡ���кͣ�˵�������Ӻ�OH�������ʵ�����ͬ����Va��0.1��Vb��0.01�����Va��Vb=1�U10��
�����Ѷȣ�һ��
3��ѡ���� 25��ʱ�������и���Һ��������ȷ����
A��pH��2��������pH��l��������Һ��c��H����֮��Ϊ2 ��1
B��4��pH��ͬ����Һ����CH3COONa��C6H5ONa��NaHCO3��NaOH������Һ�����ʵ���Ũ���ɴ�С��˳���Ǣ�>��>��>��
C��0��1 mol/LHA��ij�ᣩpH��3��0��1 mol/L BOH��ij�pH��13����BA���Σ�����ҺpH<7
D��pH��3�Ĵ�����Һ��pH��11��NaOH��Һ�������ϣ�c��Na��>c��CH3COO��>c��H��>c��OH�� 2010��֣�ݸ��б�ҵ�����������Ԥ�����ۻ�ѧ����
�ο��𰸣�D
�����������
�����Ѷȣ���
4��ѡ���� ij�¶�����ˮ�д������µ���ƽ�⣺D2O  ?D++OD-��Kw��D2O��=1.0��10-12����pD=-lg{c(D+)},����¶����йط�������ȷ���ǣ�?��
?D++OD-��Kw��D2O��=1.0��10-12����pD=-lg{c(D+)},����¶����йط�������ȷ���ǣ�?��
A 0.1 molNaOD ������ˮ�γ�1L��Һ����pD=11
B��pD=4��DCl����ˮ��Һ������ˮϡ��100����?��pD=6
C ��30 ml 0.5mol/L NaOD ����ˮ��Һ�м���20ml? 0.5mol/LDCl����ˮ��Һ��������Һ��pD=11
D pD=10��NaOD��ˮ��Һ�У�����ˮ�������C��OD-��=1��10-10mol/L
�ο��𰸣�B
�������������ˮ�ڸ��¶��µ�PD=6Ϊ���ԣ���PDС��6��Һ�����ԣ�����6�ʼ��ԣ�����
A��ȷ������ˮ�ڸ��¶��µ�PD=6Ϊ���ԣ����ԣ�0.1 molNaOD ������ˮ�γ�1L��Һ����pD=11��B����DCLΪ�ᣬ��������ϡ�;������ܳ�����PD=6��C��ȷ��D��ȷ��
�����Ѷȣ�һ��
5��ѡ���� pH��1����������ҺA��B��C��1 mL���ֱ��ˮϡ�͵�1000 mL����pH����Һ���(V)�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����(����)
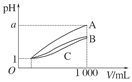
A����Һ�����ʵ���Ũ��C>B>A
B������A>B>C
C����a��4����A��ǿ�ᣬB��C������
D����1<a<4����A��B��C��������
�ο��𰸣�B
�����������ͬpH�����ϡ����ͬ����ǿ��pH�仯��ͼ���ѵó����ԣ�B��CӦ����ͬ��Ũϡ���������B�����
�����Ѷȣ�һ��