微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中各微粒的浓度关系不正确的是
A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4的溶液中,c(NH4+)大小:①=②>③
B.常温下,在10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL
C.25℃时,浓度均为0.1 mol・L-1的NH3・H2O、NH4Cl溶液等体积混合,所得溶液显碱性:c(NH4+)+c(H+)>c(NH3・H2O)+c(OH-)
D.浓度均为0.1mol/L的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
参考答案:D
本题解析:pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,NH4HSO4电离出H+,NH4+浓度最小,NH4Cl和(NH4)2SO4水解程度相同,则c(NH4+)相同,正确顺序为①=②>③,故A正确;选项B中如果HA是强酸,则消耗HA的溶液体积是10ml。如果HA弱酸,则消耗HA的溶液体积小于10ml,B正确;C中溶液显碱性,说明氨水的电离程度大于NH4+的水解程度,则c(Cl-)>c(NH3・H2O)。根据电荷守恒可知,c(NH4+)+c(H+)=c(Cl-)+c(OH-),因此c(NH4+)+c(H+)>c(NH3・H2O)+c(OH-),C正确;D中根据电荷守恒可知,c(CH3COO-)+ c(OH-)=c(Na+)+c(H+),根据物料守恒可知2c(Na+)=c(CH3COOH)+c(CH3COO-),则c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-),D不正确,答案选D。
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合题意灵活运用即可。
本题难度:简单
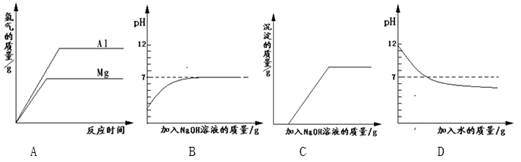
2、选择题 下列实验对应的图象正确的是
 ?
?
A.将等质量的镁和铝分别与足量的盐酸反应
B.向pH=2的盐酸中滴加过量的氢氧化钠溶液
C.向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液
D.向pH=12的氢氧化钠溶液中加水稀释
参考答案:C
本题解析:A项:镁比铝活泼,镁的图线角度要大,故错;B项:氢氧化钠过量,最终溶液呈碱性,故错;D项:碱稀释不会变成酸,故错。故C。
点评:本题考查的是化学图像综合分析的相关知识,题目难度不大,注意碱再稀释也不会变成算。
本题难度:简单
3、选择题 下列溶液肯定显酸性的是(?)
A.含H+的溶液
B.c(H+)=1×10-7mol・L-1
C.pH<7的溶液
D.c(OH-)<c(H+)的溶液
参考答案:C
本题解析:只要溶液中氢离子浓度大于OH-浓度,溶液就显酸性,所以选项D一定是正确的,其余不一定,答案选C。
本题难度:简单
4、选择题 下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol・L-1 Na2S溶液中一定有:c(OH-)= c(H+)+ c(HS-)+2c(H2S)
B.向NH4Cl溶液中加入适量氨水,得到的碱性混合溶液中一定有 :
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.加热Na2S溶液,溶液c(OH-)肯定增大,c(H+)肯定减小
D.加水稀释0.1mol・L-1醋酸溶液,电离平衡向右移动,c(H+)一定减小
参考答案:AD
本题解析:A 正确,遵循质子守恒
B 错误,如果离子浓度存在这种关系的话,溶液就带负电了。
C 错误,加热Na2S溶液,硫离子水解程度增大,c(OH-)肯定增大,但KW也增大了,c(H+)就不一定增大了。
D 正确,加水稀释,醋酸的电离平衡向右移动,但体积增大了,c(H+)就一定减小。
本题难度:简单
5、选择题 已知反应:下列结论正确的是
[? ]
①101KPa时,2C(s)+O2(g)=2CO(g);ΔH=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3kJ/mol
A.碳的燃烧热大于110.5kJ/mol
B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
参考答案:A
本题解析:
本题难度:简单