微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若在宇宙飞船的太空实验室(失重条件下)进行以下实验,其中最难完成的是
[? ]
A.将金粉和铜粉混合
B.将牛奶加入水中混合
C.蒸发食盐水得到食盐固体
D.用漏斗、滤纸过滤除去水中的泥沙
参考答案:D
本题解析:
本题难度:一般
2、填空题 纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2・xH2O,经过滤,水洗除去其中的Cl-再烘干、焙烧除去水分得到固体TiO2。用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定
Ti3+至全部生成Ti4+。请回答下列问题:
(1)TiCl4水解生成TiO2・xH2O的化学方程式为______________________________。
(2)检验TiO2・xH2O中Cl-是否被除净的方法是______________________________。
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是___________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的________(填字母代号)。
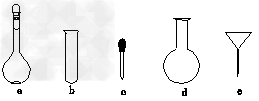
(4)滴定终点的现象是_________________________。
(5)滴定分析时,称取TiO2(摩尔质量为M?g/mol)试样w?g,消耗c?mol/L?NH4Fe(SO4)2标准溶液V?mL,则TiO2质量分数表达式为______________________________________。
(6)判断下列操作对TiO2质量分数测定结果的影响(填“偏高”“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果______。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果________。
参考答案:(1)TiCl4+(x+2)H2O TiO2・xH2O↓+4HCl
TiO2・xH2O↓+4HCl
(2)取少量水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除尽
(3)抑制NH4Fe(SO4)2水解;a、c
(4)溶液变为红色
(5)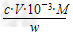 ×100%
×100%
(6)①偏高;②偏低
本题解析:
本题难度:一般
3、选择题 海带中含有碘离子,某化学兴趣小组设计如下的步骤从海带中提取单质碘: ①通足量氯气 ②将海带烧成灰,向灰中加水搅拌 ③加CCl4振荡 ④过滤 ⑤用分液漏斗分液。合理的操作顺序为
[? ]
A.①→③→⑤→②→④
B.②→①→③→④→⑤
C.②→④→①→③→⑤
D.③→①→②→⑤→④
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列实验装置及操作正确的是( )
A.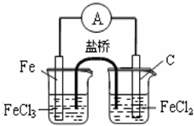
构成原电池
B.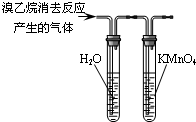
检验溴乙烷消去后的产物是否含乙烯
C.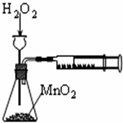
测定H2O2的分解速率
D.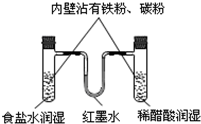
研究钢铁的析氢腐蚀和吸氧腐蚀
参考答案:B
本题解析:
本题难度:简单
5、简答题 为了用实验的方法验证镁和铁的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铁与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铁与稀盐酸反应的情况
回答下列问题:
(1)以上两实验方案实验现象较为明显的是方案______
(2)学生乙在实验中取了一段镁条,投入稀盐酸中,现象不是十分明显,请分析原因______.
(3)学生丙另辟蹊径,仅用镁条、铁片与盐酸只进行一次实验也得出正确的结论(其它用品自选),学生丙用的是什么方法?______简述现象______.
参考答案:(1)常温下金属镁和水的反应不是很剧烈,金属铁和水不反应,但是二者均可以和盐酸反应,并且金属镁和酸反应产生氢气的速率快,剧烈,而金属铝不如镁剧烈,故答案为:方案二;
(2)在金属镁条的表面会生成一层致密的氧化物薄膜,阻止一些反应的进行,这样导致镁条投入稀盐酸中,现象不是十分明显,故答案为:镁的表面存在氧化膜;
(3)原电池中负极金属的活泼性一般是强于正极金属的活泼性的,这样让金属镁和铁做电极,让盐酸作电解质,会在金属铁电极表面产生气泡,所以金属铝是正极,镁条溶解,镁是负极,活泼性:金属镁强于金属铝,
故答案为:构成原电池的方法;镁条溶解,铁的表面有气泡.
本题解析:
本题难度:一般