��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʾ����ڳ��������У����ױ��ʵ���
A.������
B.������
C.̼����
D.������
�ο��𰸣�C
������������������ݸ����ʾ����ڳ��ڵ������У����ʱ����Ƿ�����ѧ�仯�������������ɣ�
���A��������ȶ��ֽܷ�����������������A����
B����������������Ӧ���������ƣ�����ˮ������Ӧ�������ƺ���������B����
C��̼�����ڿ����л����ޱ仯����C��ȷ��
D���������ڿ����л���ˮ������Ӧ�����������ƣ���������̼��ƣ���D����
��ѡ��C��
������������Ҫ���������ʵĻ�ѧ���ʣ����ʱ����Ƿ�����ѧ�仯���������������ǽ���Ĺؼ���
�����Ѷȣ�����
2��ѡ���� ���з�Ӧ�����ڻ��Ϸ�Ӧ��������������ԭ��Ӧ����
A.Fe+2HCl=FeCl2+H2��
B.2FeCl2+Cl2=2FeCl3
C.CaO+H2O=Ca��OH��2
D.2Fe��OH��3Fe2O3+3H2O
�ο��𰸣�B
������������������Ϸ�Ӧ�����ֻ��������ϵķ�Ӧ������һ�ֲ���ķ�Ӧ���л��ϼ۱仯�ķ�Ӧ��������ԭ��Ӧ���ݴ˷����жϣ�
���A��Fe+2HCl=FeCl2+H2���У���Ӧǰ��������Ԫ�صĻ��ϼ۱仯�����Ը÷�Ӧ��������ԭ��Ӧ�����÷�Ӧ�����û���Ӧ���ǻ��Ϸ�Ӧ����A����
B��2FeCl2+Cl2=2FeCl3�У��÷�Ӧ����������������һ�����ʣ��ҷ�Ӧǰ��������Ԫ�صĻ��ϼ��б仯�����Ը÷�Ӧ����������ԭ��Ӧ���ǻ��Ϸ�Ӧ����B��ȷ��
C��CaO+H2O=Ca��OH��2�У��÷�Ӧ����������������һ���������ڻ��Ϸ�Ӧ������Ӧǰ���Ԫ�صĻ��ϼ۲��䣬���Բ���������ԭ��Ӧ����C����
D��2Fe��OH��3 Fe2O3+3H2O�У��÷�Ӧ����һ���������������������ڷֽⷴӦ���ҷ�Ӧǰ���Ԫ�صĻ��ϼ۲��䣬���Բ���������ԭ��Ӧ����D����
Fe2O3+3H2O�У��÷�Ӧ����һ���������������������ڷֽⷴӦ���ҷ�Ӧǰ���Ԫ�صĻ��ϼ۲��䣬���Բ���������ԭ��Ӧ����D����
��ѡB��
���������⿼��������ԭ��Ӧ�ͻ��Ϸ�Ӧ���жϣ��ѶȲ���ע��������ԭ��Ӧ����������Ԫ�ػ��ϼ۵ı仯��
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��ȷ����
A.ͭ����������Һ��Ӧ��Cu+Ag+�TCu2++Ag
B.��������Һ������������Һ�ķ�Ӧ��Ba2++SO42-�TBaSO4
C.����ϡ���ᷴӦ��2Fe2++6H+�T2Fe3++3H2
D.̼��ƺ�ϡ���ᷴӦ��CO32-+2H+�TCO2+H2O
�ο��𰸣�B
���������������A����ɲ��غ㣻
B�������ƺ�����������Һ��Ӧ�������ᱵ������
C�������ʺ�ϡ�ᷴӦ�����������ӣ�
D��̼������������ʣ�
���A��ͭ����������Һ��Ӧ���ӷ���ʽΪ��Cu+2Ag+�TCu2++2Ag����A����
B����������Һ������������Һ�ķ�Ӧ�����ӷ���ʽΪ��Ba2++SO42-�TBaSO4������B��ȷ��
C������ϡ���ᷴӦ�����ӷ���ʽΪ��Fe+2H+�TFe2++H2������C����
D��̼��ƺ�ϡ���ᷴӦ���ӷ���ʽΪ��CaCO3+2H+�TCO2��+H2O+Ca2+����D����
��ѡB��
���������⿼�������ӷ���ʽ����д������ע�����⣬��Ҫ�������ӷ���ʽ�ĵ���غ㣬���Ϸ�Ӧԭ�������ܵ���ʲ��ܲ��ԭ�ϼ�
�����Ѷȣ�����
4��ѡ���� �������ӷ���ʽ��д��ȷ����
A.�Ȼ�������Һ������������Ӧ��2?Fe2++Cl2=2?Fe3++2?Cl?-
B.��̼��������Һ�еμ�����ϡ���CO32-+2H?+=CO2��+H2O
C.ͭ��ϡ���ᷴӦ��Cu+4H++2NO3-=Cu2++2?NO2��+2H2O
D.̼�������Һ����������������Һ��Ӧ��NH4++OH?-=NH3?H2O
�ο��𰸣�A
���������������A����Ӧ�����Ȼ���������Ӧ������ѧʽ��
B��̼��������Ӳ��ܲ�֣�
C����Ӧ����NO��
D��©д̼������������ķ�Ӧ��
���A���Ȼ�������Һ������������Ӧ�����ӷ�ӦΪ2Fe2++Cl2=2Fe3++2Cl?-����A��ȷ��
B����̼��������Һ�еμ�����ϡ��������ӷ�ӦΪHCO3-+H+=CO2��+H2O����B����
C��ͭ��ϡ���ᷴӦ�����ӷ�ӦΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O����C����
D��̼�������Һ����������������Һ��Ӧ�����ӷ�ӦΪHCO3-+NH4++2OH-=NH3?H2O+CO32-+H2O����D����
��ѡA��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ���ע�����ӷ�Ӧ����д������������������ԭ��Ӧ���ɽ����Ŀ�ѶȲ���
�����Ѷȣ���
5��ѡ���� 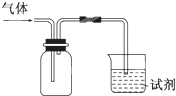 ��ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ���ʣ�����˵����ȷ����
��ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ���ʣ�����˵����ȷ����
A.A
B.B
C.C
D.D
�ο��𰸣�B
���������������A����������ʹ���������Һ�����ֵ��Ƕ�������Ļ�ԭ�ԣ�
B����������ʹƷ����ɫ�����ֶ��������Ư���ԣ�
C���������������������ܷ�Ӧ��������������
D����Ϊ���������Ư����һ����ѡ���ԣ�����Ư��ʯ��ȣ����������ԣ����������˵û��Ư���ԣ�
���A�����Ը�������ܽ�����������ˮ��Һ�����������ᣬ������ԭΪ��ɫ�Ķ��������ӣ������Ը�����ص������Ե����֣��������ֵ��Ƕ�������Ļ�ԭ�ԣ���A����
B��ʹƷ����Һ��ɫ��������Ӧ���������ɲ��ȶ��Ļ�������Ⱥ��ָֻ�Ϊԭ���ĺ�ɫ�������˶��������Ư���ԣ���B��ȷ��
C����������Ϊ����������ܸ��������Ʒ�Ӧ�����������ƺ�ˮ��������������C����
D����������ʹ��ɫʯ����Һ������ɫ�����������ԣ����������˵û��Ư���ԣ���Ϊ���������Ư����һ����ѡ���ԣ�����Ư��ʯ��ȣ���D����
��ѡB��
���������⿼�������������ʣ���������Ϊ������������������������ͨ�ԣ�����������Ư���ԡ�ǿ��ԭ�Ե��������ԣ����������Ư����ѡ���ԣ�
�����Ѷȣ�һ��