|
高中化学知识点讲解《反应速率与平衡的有关计算》高频考点预测(2017年最新版)(八)
2017-07-10 20:26:18
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 铁及其化合物在生产、生活中应用广泛。
(1)一定条件下,Fe与CO2可发生反应:
2Fe(s)+3CO2(g) Fe2O3(s)+3CO(g) Fe2O3(s)+3CO(g)
该反应的平衡常数(K ) 随温度(T ) 升高而增大。
①该反应的平衡常数K=______。(填表达式)
②下列措施中,能使平衡时c(CO)/c(CO2) 增大的是?(填标号)。
A.升高温度
B.增大压强
C.充入一定量CO
D.再加一些铁粉
| (2)图1装置发生反应的离子方程式为?。

(3)图2装置中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。

① 电源的M端为?极,甲烧杯中铁电极的电极反应为?。
② 乙烧杯中电解反应的化学方程式为?。
③ 停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g,甲烧杯中产生的气体标准状况下体积为?mL 。
参考答案:(1)①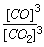 (2分)?②A?(2分) (2分)?②A?(2分)
(2)2Fe3++Cu =2Fe2++Cu2+(2分)
(3)①正(2分),? Fe - 2e-=Fe2+(2分)
②2CuSO4+2H2O 2Cu +O2↑ +2H2SO4?(3分)?③224(3分) 2Cu +O2↑ +2H2SO4?(3分)?③224(3分)
本题解析:(1)①Fe与Fe2O3为固体,不列入平衡常数表达式。
②升高温度,平衡向右移动,c(CO)/c(CO2) 增大,A项正确;,因为反应前后气体系数相等,增大压强、充入一定量CO, c(CO)/c(CO2)不变,故B项、C项不正确;再加铁粉,平衡不移动,D项不正确。
(3)①石墨电极附近变红,H2O电离出的H+放电,使OH?浓度增大,该电极为阴极,所以N极为负极,M极为正极;甲烧杯中铁电极为阳极,Fe失电子:Fe - 2e-=Fe2+。
②电解CuSO4溶液生成Cu、O2、H2SO4,方程式为:2CuSO4+2H2O 2Cu +O2↑ +2H2SO4。 2Cu +O2↑ +2H2SO4。
③Cu电极:Cu2++2e?=Cu,n(e?)=2n(Cu2+)=2×0.64g÷64g/mol=0.02mol,串联电路中通过的电量相等,甲烧杯中石墨电极产生H2:2H++2e?=H2↑V(H2)=1/2n(e?)×22.4L/mol=0.224L=224ml。
本题难度:一般
2、计算题 在2L的密闭容器中充入一定量的SO3,在一定温度和催化剂作用下,发生反应:2SO3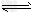 2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求: 2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求:
(1)n(SO2);
(2)氧气的生成速率v?(O2);
(3)SO3的转化率;
参考答案:(1)1.6mol
(2)v?(O2)=0.1?mol?/(L・min)
(3)20%
本题解析:
本题难度:一般
3、填空题 (15分)已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)可逆反应FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表: Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
?
①写出该反应平衡常数的表达式__________。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量_____;充入氦气,混合气体的密度____(选填“增大”、“减小”、“不变”)。
(2)常温下,浓度均为0.1 mol・L-1的下列六种溶液的pH如下表:
溶质
| CH3COONa
| NaHCO3
| Na2CO3
| NaClO
| NaCN
| C6H5ONa
| pH
| 8.8
| 9.7
| 11.6
| 10.3
| 11.1
| 11.3
|
①上述盐溶液中的阴离子,结合质子能力最强的是?
②根据表中数据判断,浓度均为0.01 mol・L-1的下列五种物质的溶液中,酸性最强的是?;
将各溶液分别稀释100倍,pH变化最小的是?(填编号)。
A.HCN?B.HClO?C.C6H5OH?D.CH3COOH ?E.H2CO3
③据上表数据,请你判断下列反应不能成立的是?(填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa? B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO?D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为?
(3)已知常温下Cu(OH)2的Ksp=2×10-20。又知常温下某CuSO4溶液里c(Cu2+)=0.02 mol・L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于?;要使0.2 mol・L-1的CuSO4溶液中Cu2+沉淀较为完全 ( 使Cu2+浓度降至原的千分之一)则应向溶液里加NaOH溶液,使溶液pH为?。
参考答案:⑴? ①k=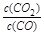 ?;②减小;增大 ?;②减小;增大
⑵? ①CO32-;②D;C;③? C D;④2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。⑶ 5; 6。
本题解析:(1)①该反应平衡常数的表达式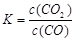 ;②由于温度升高,化学平衡常数减小。说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应。若升高温度,平衡逆向移动,气体的质量减小,而气体的物质的量不变,所以混合气体的平均相对分子质量减小;充入氦气,化学平衡不发生移动,但在整个容器内气体的质量增大,所以混合气体的密度增大;(2)①同种浓度的离子结合质子能力越强,则盐水解程度就越大,盐溶液的碱性就越强,即pH越大。由于Na2CO3溶液的pH最大,说明CO32-与H+结合力最强。因此上述盐溶液中的阴离子,结合质子能力最强的是CO32-。③发生反应时应该是强酸制取弱酸。A.酸性CH3COOH> H2CO3,正确。B.酸性CH3COOH> HCN.正确。C. H2CO3>HClO。正确。D.由于酸性:H2CO3>C6H5OH> HCO3-,所以会发生反应CO2+H2O+C6H5ONa=NaHCO3+C6H5OH。错误。④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为:2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。(3)c (Cu2+)・c2(OH-)≥Ksp=2×10-20; c2(OH-)≥2×10-20÷0.02=1×10-18; c(OH-)≥1×10-9;所以pH=5; c(Cu2+)= 0.2 mol/L÷1000=2×10-4mol/L,则c2(OH-)≥2×10-20÷2×10-4mol/L=1×10-16,所以c(OH-)≥1×10-8;pH=6. ;②由于温度升高,化学平衡常数减小。说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应。若升高温度,平衡逆向移动,气体的质量减小,而气体的物质的量不变,所以混合气体的平均相对分子质量减小;充入氦气,化学平衡不发生移动,但在整个容器内气体的质量增大,所以混合气体的密度增大;(2)①同种浓度的离子结合质子能力越强,则盐水解程度就越大,盐溶液的碱性就越强,即pH越大。由于Na2CO3溶液的pH最大,说明CO32-与H+结合力最强。因此上述盐溶液中的阴离子,结合质子能力最强的是CO32-。③发生反应时应该是强酸制取弱酸。A.酸性CH3COOH> H2CO3,正确。B.酸性CH3COOH> HCN.正确。C. H2CO3>HClO。正确。D.由于酸性:H2CO3>C6H5OH> HCO3-,所以会发生反应CO2+H2O+C6H5ONa=NaHCO3+C6H5OH。错误。④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为:2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。(3)c (Cu2+)・c2(OH-)≥Ksp=2×10-20; c2(OH-)≥2×10-20÷0.02=1×10-18; c(OH-)≥1×10-9;所以pH=5; c(Cu2+)= 0.2 mol/L÷1000=2×10-4mol/L,则c2(OH-)≥2×10-20÷2×10-4mol/L=1×10-16,所以c(OH-)≥1×10-8;pH=6.
本题难度:一般
4、填空题 已知下列两个反应:
反应Ⅰ:CO2(g)+H2(g)  CO(g)+H2O ΔH1 CO(g)+H2O ΔH1
反应Ⅱ:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH2 CO2(g)+H2(g) ΔH2
(1)相同温度下,若上述反应Ⅰ的化学平衡常数为K1,反应Ⅱ的化学平衡常数为K2,那么K1・K2=________。
(2)反应Ⅰ化学平衡常数K1和温度t的关系如下表一:
t/℃
| 700
| 800
| 850
| 1 000
| 1 200
| K1
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
?
该反应的ΔH1__________0(选填“>”、“=”或“<”)。
(3)某温度下,反应Ⅰ的化学平衡常数为2.25。在该温度下,向甲、乙、丙三个恒容密闭容器中通入CO2(g)和H2(g),这两种物质的起始浓度如下表二:
起始浓度
| 甲
| 乙
| 丙
| c(CO2)(mol/L)
| 0.01
| 0.02
| 0.02
| c(H2)(mol/L)
| 0.01
| 0.01
| 0.02
|
?
反应速率最快的是________(填“甲”、“乙”或“丙”),平衡时,H2转化率最大的是________(填“甲”、“乙”或“丙”),丙中H2的转化率为________。
参考答案:(1)1 (2)> (3)丙 乙 60%
本题解析:(1)反应Ⅰ和反应Ⅱ是一个反应,而且温度相同,只是表达方式有差别,反应Ⅰ的反应物是反应Ⅱ的生成物,故K1与K2互为倒数的关系。
(2)由表中温度与化学平衡常数的关系可知,温度越高,化学平衡常数(K)越大,即升高温度,平衡向正反应方向移动,故正反应为吸热反应,ΔH>0。
(3)丙中的CO2(g)和H2(g)起始浓度都最大,而反应温度相同,故丙中反应速率最大。甲、丙为等效平衡,而乙中CO2(g)的浓度大于H2(g)的浓度,故乙中H2转化率最大。
设丙中平衡时CO(g)的浓度为x mol/L,那么CO2(g)的浓度为(0.02 -x)mol/L,H2(g)的浓度为(0.02-x)mol/L,H2O(g)的浓度为x mol/L,
所以K=x2/(0.02-x)2=2.25,解得x=0.012,
即H2(g)的浓度为0.008 mol/L,
故丙中H2的转化率为×100%=60%。
本题难度:一般
5、选择题 440℃时2SO2(g) + O2(g) 2SO3(g) △H=-198kJ/mol,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),经5min达到平衡。其起始物质的量及SO2的平衡转化率如下表所示。 2SO3(g) △H=-198kJ/mol,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),经5min达到平衡。其起始物质的量及SO2的平衡转化率如下表所示。
?
| 甲
| 乙
| 丙
| 起始物质的量
| n(SO2) / mol
| 0.4
| 0.8
| 0.8
| n(O2) / mol
| 0.24
| 0.24
| 0.48
| SO2的平衡转化率
| 80%
| α1
| α2
|
下列判断中,错误的是
A.甲中SO2的速率为0.032mol・L-1・min-1?B.440℃时,平衡常数K=400
C.温度高于440℃时,平衡常数K>400? D.平衡时,SO2的转化率:α1<80%<α2
参考答案:C
本题解析:A、平衡时消耗SO2的物质的量是0.4mol×0.8=0.32mol,浓度是0.32mol÷2L=0.16mol/L,因此甲中SO2的速率为0.16mol/L÷5min=0.032mol・L-1・min-1,A不正确;B、平衡时SO2的浓度是0.08mol/L÷2L=0.04mol/L,三氧化硫的浓度是0.16mol/L,氧气的浓度是(0.24mol-0.16mol)÷2L=0.04mol/L,所以该温度下反应的平衡常数K=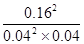 ?=400,B正确;C、正方应是放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,C不正确;D、乙容器相当于是在甲容器的基础上增大二氧化硫的浓度,二氧化硫的转化率降低;丙容器相当于是在甲容器的基础上增大压强,平衡向正反应方向移动,二氧化硫的转化率增大,D正确,答案选C。 ?=400,B正确;C、正方应是放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,C不正确;D、乙容器相当于是在甲容器的基础上增大二氧化硫的浓度,二氧化硫的转化率降低;丙容器相当于是在甲容器的基础上增大压强,平衡向正反应方向移动,二氧化硫的转化率增大,D正确,答案选C。
本题难度:一般
| 
