微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为了治理废水中Cr2O72-的污染,常先加入试剂使之变为Cr3+,该试剂为
A.NaOH溶液
B.FeCl3溶液
C.明矾
D.Na2SO3和H2SO4
参考答案:D
本题解析:从重铬酸根到三价铬离子,被还原,需要加入还原剂。故只有D符合。
本题难度:一般
2、选择题 常温下0.2mol/L HCN和0.1mol/L NaOH等体积混合后溶液pH>7,混合溶液中有关粒子物质的量浓度关系正确的是
A.c(HCN)+c(CN-)=c(Na+)
B.c(HCN)+2c(H+)=2c(OH-)+c(CN-)
C.c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+)
D.c(HCN)>c(CN-)>c(Na+)>c(H+)>c(OH-)
参考答案:CB
本题解析:本题考查离子浓度大小的关系,属中档题。反应后的混合物溶液中为1:1的HCN和NaCN,因pH>7,故D项错。A项的物料守恒应为:c(HCN)+c(CN-)=2c(Na+)①,故错;溶液中的电荷守恒关系是c(Na+) +c(H+)=c(OH-)+c(CN-) ②,将①+②×2得,B项正确。由题意知,CN-的水解能力大于HCN的电离,即CN-+H2O
②,将①+②×2得,B项正确。由题意知,CN-的水解能力大于HCN的电离,即CN-+H2O HCN+OH-与HCN
HCN+OH-与HCN H++CN-比,前者程度大,所以c(HCN)> c(CN-)
H++CN-比,前者程度大,所以c(HCN)> c(CN-) ,结合①得,c(Na+)介于两者中间,故C项正确。
,结合①得,c(Na+)介于两者中间,故C项正确。
本题难度:一般
3、填空题 (12分)下图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用下式表示:
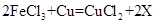 .
.

(1)上式中X物质的化学式为 。
(2)在上述反应中,氧化剂为 ,氧化产物为 ,
将两者的氧化性比较, 的氧化性更强。
(3)用双线桥法表示该反应的电子转移情况 。
(4)该反应的离子方程式为 。
参考答案:
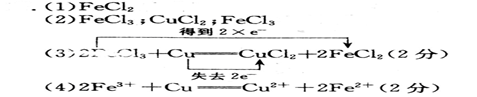
本题解析: (1)根据原子守恒可知2X含有2个Fe,4个Cl,故X为FeCl2;(2)反应中,FeCl3中Fe元素的化合价由+3价降低为+2价,FeCl3为氧化剂,被还原,对应的还原产物为FeCl2,Cu元素的化合价升高,由0价升高为+2价,为还原剂,被氧化物,对应的氧化产物为CuCl2;根据氧化剂的氧化性大于氧化产物的氧化性,可得氧化性:FeCl3>CuCl2;(3)反应Cu+2FeCl3
本题难度:一般
4、选择题 人体正常的血红蛋白中含有亚铁离子,若误食亚硝酸盐,则使血红蛋白中亚铁离子转化为铁离子而丧失其生理功能,临床证明服用维生素C可以解毒,这说明维生素C具有( )
A.酸性
B.碱性
C.还原性
D.氧化性