微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 具有相同电子层数的X、Y、Z三种元素,已知它们最高价氧化物对应的水化物的酸性强弱顺序是HXO4>H2YO4>H3ZO4,则下列判断正确的是
A.原子半径:X>Y>Z
B.元素的非金属性:X>Y>Z
C.气态氢化物的稳定性:HX<H2Y<ZH3
D.阴离子的还原性:X->Y2->Z3-
参考答案:B
本题解析:根据元素周期律题目所给条件,可以举特例X、Y、Z三种元素分别为:Cl、S、P,然后对各选项进行比较.选项A中,应为Z>Y>X;选项C中,应为ZH3<XH2<HY;选项D中,应为Z3->Y2>X-,故答案:选B项.
本题难度:困难
2、推断题 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为
51;Y 原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_______、_______;杂化轨道分别是____、____ ;a分子的立体结构是_______。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)_______。
(4)Y与Z比较,电负性较大的________,W的+2价离子的核外电子排布式是_______。
参考答案:(1)CH4;SiH4;sp3;sp3;正四面体
(2)分子;原子
(3)CO2
(4)C;1s22s22p63s23p63d10
本题解析:
本题难度:一般
3、选择题 已知X、Y、Z为同周期三种原子序数相连的短周期元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4则下列说法正确的是( )
A.原子序数:Z>Y>X
B.非金属活泼性:Y<X<Z?
C.原子半径:X>Y>Z?
D.气态氢化物的稳定性:HX>H2Y>ZH3?
参考答案:D
本题解析:
本题难度:一般
4、填空题 19世纪中叶,门捷列夫总结出了如下表所示的元素化学性质的变化规律。请回答
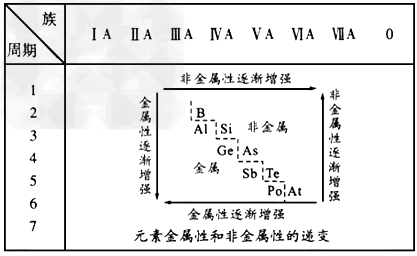
(1)门捷列夫的突出贡献是_______。 ?
A.提出了原子学说?B.提出分子学说 ?C.发现元素周期律?D.发现能量守恒定律
(2)该表变化表明_______。 ?
A.物质的性质总是在不断变化的 ?
B.元素周期表中最右上角的氦元素是非金属性最强的元素 ?
C.第IA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强 ?
D.物质发生量变到一定程度必然引起质变 ?
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到_______。 ?
A.耐高温材料?B.新型农药材料 ?C.半导体材料?D.新型催化剂材料 ?
(4)据报道,美国科学家制得一种新原子283116X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是_______。 ?
A.这种原子的中子数为167 ?B.它位予元素周期表中第六周期 ?
C.这种元素一定是金属元素 ?D.这种元素的原子易与氢化合
参考答案:(1)C?
(2)D?
(3)C?
(4)AC
本题解析:
本题难度:一般
5、选择题 下列的氢氧化物中,碱性最强的是( )
A.Ca(OH)2
B.NaOH
C.RbOH
D.Al(OH)3
参考答案:由元素在周期表中的位置及同主族从上到下元素的金属性增强,同周期从左向右元素的金属性减弱,
则金属性Rb>Ca>Na>Al,
元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,
所以RbOH的碱性最强,
故选C.
本题解析:
本题难度:一般