微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)Ⅰ.在用稀硫酸与锌制取氢气的实验中,加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)加入少量硫酸铜溶液可以加快氢气生成速率的原因是?;
(2)要加快上述实验中气体产生的速率,还可采取的措施有?(答两种);
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,某学习小组设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
?实验
混合溶液
| A
| B
| C
| D
| E
| F
|
4 mol・L-1H2SO4?/ mL
| 30
| V1
| V2
| V3
| V4
| V5
|
?饱和CuSO4溶液 / mL
| 0
| 0.5
| 2.5
| 5
| V6
| 20
|
H2O / mL
| V7
| V8
| V9
| 15
| 10
| 0
|
?请完成此实验设计,其中:V2 ?V5 =?, V6=?,V8=?;
(第一空填“>”、“<”或“=”;后三空填具体数值)
Ⅱ.常温下,某一元酸HA和NaOH溶液等体积混合,HA和NaOH的浓度以及混合后溶液的pH如下表:
组别
| c(HA)/mo1・L-1
| c(NaOH)/mo1・L-1
| 混合液pH
|
甲
| c
| 0.2
| pH = 7
|
乙
| 0.2
| 0.1
| pH>7
|
丙
| 0.1
| 0.1
| pH = 9
|
请回答下列问题:
(4)仅从甲组情况分析,c是否一定等于0.2 ??(选填“是”或“否”)。
(5)分析乙组实验数据,HA是?酸(选填“强”或“弱”)。该混合液中离子浓度由大到小的顺序是?。
(6)丙组所得混合液中由水电离出的c(OH-) =?mo1・L-1。
参考答案:(14分)
 Ⅱ.(4)否(1分);
Ⅱ.(4)否(1分);
(5)弱(1分);c(Na+)>c(A-)>c(OH-)>c(H+)(或 [Na+]>[A-]>[OH-]>[H+])(2分)
(6)10-5?(2分);
本题解析:(1)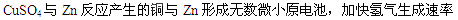
(2)加快化学反应的速率的因素有:升高温度、加入催化剂、增大压强(有气体参加的反应)、增大反应物的浓度、反应物的接触面积大小等,本题可采用的措施有:
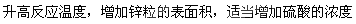
(3)该实验的目的为:研究硫酸铜的量对氢气生成速率的影响,所以所取硫酸的量就是相同的,即V2=V5 =30;
由所加饱和CuSO4溶液的数据分析可得:V6=10;比较D、E、F中饱和CuSO4溶液的体积与所加水的体积分析可知,饱和CuSO4溶液的体积与加入水的体积和为20,进而求得V8=19.5;
(4)对于甲组来说,溶液的pH = 7为中性溶液,但无法确定c是否一定等于0.2,HA可以为弱酸,也可以为强酸;
(5)由乙组数pH>7,溶液呈碱性,且在等体积混合的情况下,HA的浓度又是NaOH溶液的2倍,即可得HA一定为弱酸。该混合体系中,溶液中的溶质为等物质的量的HA、NaA,
溶液中的离子成分为:Na+、A-、H+、OH-四种成分,由于溶液呈碱性,即以A-水解为主HA电离为次,所以溶液中各离子浓度的大小关系为:c(Na+)>c(A-)>c(OH-)>c(H+)
(6)丙组为等体积等物质的量浓度的一元酸与一元碱混合,混合后溶液中的溶质为NaA,因溶液的pH = 9,即HA为弱酸,A-水解使溶液呈碱性,促进水的电离。水电离出的c(OH-) =10-5
本题难度:简单
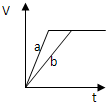
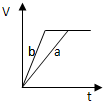
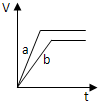
2、选择题 等质量的两份锌粉a和b,分别加入过量的稀硫酸中,并向a中加入少量氧化铜,下图表示产生H2的体积(V)与时间(t)的关系正确的是( )
A.
B.
C.
D.
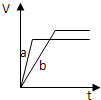
参考答案:锌和硫酸反应,加入硫酸铜溶液后,锌和铜离子反应置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属锌和硫酸反应的速率,所以反应速率是:a>b,
速率越大,锌完全反应时所用的时间越短,所a所用的时间小于b的时间;
产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,所以和硫酸反应生成氢气的量减少,所以氢气的体积是:a<b.
故选D
本题解析:
本题难度:一般
3、选择题 在化学反应A(g)+3B(g) 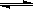 2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是( )
2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是( )
A.vA=vB
B.vA=2vC
C.vB=3vD
D.3vB=vC