| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ�ԭ���ԭ�������⼼�ɣ�2017�����°棩(��)
�ο��𰸣�D ���������A�Zn��Fe���ã�Zn�Ǹ������ʴ���B�û�����ݳ���˵��û��SO2��CO2���ɣ�KMnO4������Һ�����ɫ���ʴ���C���ʼ��Ӧ����ǿ���������泥�������Ӧ��ǿ���ʴ�����ѡD�� �����Ѷȣ��� 2��ʵ���� Al��Mg�ڲ�ͬ�ĵ������Һ�зֱ�ԭ���A��B������ͼ��ʾ: �ο��𰸣��������٣���þ���������ϣ��³��������������ϡ����ڣ��أ�����2H++2e��=H2��������Mg��2e��=Mg2+���³أ�����6H2O+6e��=3H2��+6OH��������2Al��6e��+8OH��=2AlO2��+4H2O���۳����ܹ�������������ԭ��Ӧ �����������A���п���ϡ���ᷢ����ѧ��Ӧ����þ����Mg+H2SO4=MgSO4+H2����2Al+3H2SO4=Al2(SO4)3+3H2������þ�Ľ��������Դ����������Ըõ���еĻ�ѧ��ӦΪMg+H2SO4=MgSO4+H2����þʧ��������ظ����������������ڣ³����ܷ����Ļ�ѧ��Ӧֻ�����ͼ�ķ�Ӧ����2Al+2NaOH+2H2O=2NaAlO2+3O2��,���Ըõ������ʧ��������ظ�������þֻ���������� �����Ѷȣ��� 3������� ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������£�N2H4���ǵ������ֳ���������ڿ�ѧ����������������Ҫ��Ӧ�á� |
�ο��𰸣���1�� ��1�֣�
��1�֣�
��2�� 2NH3+NaClO��N2 H4+NaCl+H2O��2�֣�
��3��N2 H4(g) + O2(g) = N2(g) + 2H2O(g ) ��H����534 kJ��mol��1��2�֣�
��1��C��2�֣�
��2��A C D��3�֣�
��3��0.3 mol��L-1��min-1��2�֣�
III��2NH3 + 6OH- + 6e- = N2 + 6H2O��2�֣�
�����������1��N2H4�е�Nԭ�ӿɴﵽ8���ӵ��ȶ��ṹ����ԭ�������3�������γ����Թ��õ��Ӷԣ���δ�ɼ���һ�Ե����γ�8�����ȶ��ṹ��ÿ����ԭ�Ӻ�������ԭ���γɹ��ۼ�����ԭ�Ӽ��γ�һ�����ۼ����ṹʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��NH3��NaClO��Ӧ�ɵõ��£�N2H4�����÷�Ӧ�Ļ�ѧ����ʽΪ��2NH3+NaClO��N2 H4+NaCl+H2O���𰸣�2NH3+NaClO��N2 H4+NaCl+H2O���Ǵ�ͼ�ж�������H=22218kJ��mol��1-2752kJ��mol��1=��534 kJ��mol��1��������ȼ��������̬ˮ���Ȼ�ѧ����ʽΪ��N2 H4(g) + O2(g) = N2(g) + 2H2O(g ) ��H����534 kJ��mol��1���𰸣�N2 H4(g) + O2(g) = N2(g) + 2H2O(g ) ��H����534 kJ��mol��1��
��A��Ӧ������֮�����жϣ���Ӧ�����а��ձ������з�Ӧ����A�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��B����������֮�ȵ���ϵ��֮�ȣ�������������Ӧ���ʣ���ij�����ʵ�����Ӧ���ʺ��淴Ӧ��������DZ�����Ӧ�ﵽƽ�⣬���Ե�3v��N2����=v��H2����?ʱ��Ӧ�ﵽƽ�⣬��B�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��C����������ѹǿ���ֲ��䣬˵����Ӧ�ﵽƽ�⣬��C���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����Ӧ��ϵ�������غ㣬���һ�����ʻ��������ܶȲ��䣬���Ի��������ܶȱ��ֲ��䣬����˵����Ӧ�ﵽƽ�⣬��D�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���𰸣�C��
��A����ȷ������1.5L�������������ҵ�Чƽ�⣬Ȼ��Ŵ�3L��ƽ��������N2�ķ����淽���ƶ�������2c1>1.5?mol��L?�D1;?B������ȷ������Ч��3molH2,1molN2����ȷ����ƽ�⣬�����1molN2��ƽ�������ƶ���C����ȷ����Ӧ��ϵ�������غ㣬���һ�����������������������ҵ�2�������Ի��������ܶȣ�2��1=��2��D����ȷ���¶Ȳ��䣬ƽ�ⳣ�����䣬K��= K��= K�����𰸣�A C D��
��v(H2)= 3v(N2)=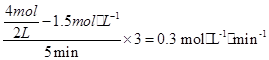 ?���𰸣�0.3 mol��L-1��min-1��
?���𰸣�0.3 mol��L-1��min-1��
III.NH3����ԭ��������1molN2ʧȥ6mol���ӣ���OH�D����ʹ����ʽ���ߵ���غ㣬������Ӧ��2NH3 + 6OH- + 6e- = N2 + 6H2O���𰸣�2NH3 + 6OH- + 6e- = N2 + 6H2O
�����Ѷȣ�һ��
4��ѡ���� һ������п�ۺ�6mol��L��1�Ĺ������ᷴӦ���������м����������������ʣ���ʯī ��CuO ��ͭ�� ��п�� ��Ũ���� ����ˮ���� ��KNO3��Һ ��CuCl2ʱ���ܹ��ӿ췴Ӧ���ʣ��ֲ������H2�������� �� ��
A���٢ۢ�
B���ڢܢ�
C���٢ۢ�
D���٢ݢ�
�ο��𰸣�C
����������ټ���ʯī�����ڹ�����ԭ��أ�Zn�����������Ի�ѧ��Ӧ���ʴ��ӿ죬�ֲ������H2������ȷ���ڼ���CuOʱ����������Cu���ʡ����ڹ�����ԭ��أ�Zn�����������Ի�ѧ��Ӧ���ʴ��ӿ죬�ֲ������H2������ȷ����ͭ�����ڹ�����ԭ��أ�Zn�����������Ի�ѧ��Ӧ���ʴ��ӿ죬�ֲ������H2��������ȷ����п�����������ʲ��䣬���Dz����������������ӣ�����Ũ���ᣬ����H+���ӣ��ܹ��ӿ췴Ӧ���ʣ��ֲ������H2��������ˮ���ᣬ����������H+����Ӧ���ʻ�ӿ죬���������ʵ���Ҳ���ӣ�����KNO3��Һ����������ᡣ����������ǿ�����ԣ�һ�㲻�ܲ�������������CuCl2ʱ���ᷢ���û���Ӧ������������Ӧ���ʻ�ӿ죬���ǣ�����������п���������������ʵ�������٣��������ѡ����C��
���㣺���������������Ի�ѧ��Ӧ���ʼ�������������ʵ�����Ӱ���֪ʶ��
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��������ʢ��ϡ���ᣬ���γ�ԭ�������Ϊ��������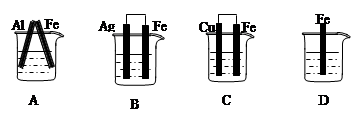
�ο��𰸣�A
���������ԭ��ص��γ�������1�������ֻ����Բ�ͬ�Ľ�����������һ��Ϊ�ǽ������壩���缫��2���缫������������Һ�У�3����������ӣ���Ӵ�����4�����Է��ķ���������ԭ��Ӧ���ݴ˿�֪ѡ��ABC�����γ�ԭ��ء����н�������Al��Fe��Cu��Ag��������ABC�����ֱ�����������������������ѡA��
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��飬�ѶȲ�������ԭ��صĹ���ԭ����ԭ��صĹ��������Ǵ���Ĺؼ���
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ����ɡ����ʵ�����.. | |
| �����Ŀ |