��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪M2O7x-+3S2-+14H+=2M3++3S��+7H2O����M2O7x-�е�M�Ļ��ϼ�Ϊ��������
A��+2
B��+3
C��+4
D��+6
�ο��𰸣�M2O7x-+3S2-+14H+=2M3++3S��+7H2O�У�
�ɵ���غ��֪��
��-x��+3����-2��+14����+1��=2����+3����
���x=2��
��M2O72-�е�M�Ļ��ϼ�Ϊy��
��y��2+��-2����7=-2��
���y=+6��
��ѡD��
���������
�����Ѷȣ�һ��
2������� ��֪ij��Ӧ�з�Ӧ�����������У�HNO3��Cu��NO3��2��NO��Cu��H2O
��1����֪Cu�ڷ�Ӧ��ʧȥ���ӣ���÷�Ӧ����������______��
��2���÷�Ӧ�У�������ԭ��Ӧ�Ĺ����ǣ�д��ѧʽ��______��______��
��3������Ӧ��Ļ�ѧʽ������ƽ���ϵ���������з����У����������ת�Ƶķ������Ŀ��
��4������1.5mol?Cu�μӷ�Ӧ����______mol?HNO3�μӷ�Ӧ������ԭ��HNO3�����ʵ�����______mol��ת�Ƶ��ӵ����ʵ�����______?mol��
�ο��𰸣���1��Cu�ڷ�Ӧ��ʧȥ���ӣ����Խ���ͭ�ǻ�ԭ����HNO3�е�NԪ�ش�����ۣ�����������������ԣ������������ʴ�Ϊ��HNO3��
��2���÷�Ӧ�ǽ���ͭ������ķ�Ӧ�����ϼ۽��͵�NԪ�ط�����ԭ��Ӧ�����������+5�۵�Ԫ�ؽ�ΪNO�е�+2�۵�Ԫ�أ��ʴ�Ϊ��HNO3��NO��
��3���÷�Ӧ�ǽ���ͭ������ķ�Ӧ�����ݵ����غ�����ƽ��ѧ����ʽΪ��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O������ת�Ƶķ������Ŀ������ʾ��
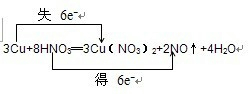
����

���ʴ�Ϊ��

��
��4�����ݻ�ѧ����ʽ���Կ���������3mol����ͭ�μӷ�Ӧʱ������8mol��������뷴Ӧ��ת�Ƶ���Ϊ6mol�����Ե���1.5mol����ͭ�μӷ�Ӧʱ������4mol��������뷴Ӧ������ԭ��HNO3�����ʵ����Dzμӷ�Ӧ�������ʵ������ķ�֮һ��������ԭ��HNO3 �����ʵ�����1mol��ת�Ƶ���Ϊ3mol���ʴ�Ϊ��4��1��3��
���������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�У�ˮ�Ȳ������������ֲ��ǻ�ԭ����������ԭ��Ӧ�ǣ�������
A��2Na+2H2O�T2NaOH+H2��
B��2F2+2H2O�T4HF+O2
C��2Na2O2+2H2O�T4NaOH+O2��
D��MgO+H2O�TMg��OH��2
�ο��𰸣�A��NaԪ�صĻ��ϼ����ߣ�HԪ�صĻ��ϼ۽��ͣ���ˮΪ����������A��ѡ��
B��FԪ�صĻ��ϼ۽��ͣ�OԪ�صĻ��ϼ����ߣ���ˮΪ��ԭ������B��ѡ��
C��ֻ�й���������OԪ�صĻ��ϼ۱仯����������ԭ��Ӧ����ˮ��H��OԪ�صĻ��ϼ۲��䣬��ˮ�Ȳ������������ֲ��ǻ�ԭ������Cѡ��
D���÷�Ӧ��û��Ԫ�صĻ��ϼ۱仯��������������ԭ��Ӧ����D��ѡ��
��ѡ��C��
���������
�����Ѷȣ���
4������� ��1��1mol��ͬ�������ʵ����������ͬ����ԭ���ǣ���______����ͬ��ͬѹʱ�κ������һ��������ͬ���Ǣ�______��
��2�������з�Ӧ����ʽ�б�������ת�Ƶķ������Ŀ�������ţ����÷�Ӧ��H2O2ֻ�������±仯���̣�H2O2��O2����______
2H2CrO4+3H2O2=2Cr��OH��3+3O2��+2H2O?�˷�Ӧ�������ɱ�״��������6.72L����ת�Ƶ��ӵ����ʵ���Ϊ��______
��3�������ʷ������������Ƴ��������Ρ��������Ρ�����������ɻ���Ϊ��______�Σ�
��4��һ��������NaHSO4��Ba��OH��2��Ӧ�����ӷ�Ӧ��дΪ��
H++SO42-+Ba2++OH-=BaSO4��+H2O����������Һ�ʢ�______�ԣ����Ի���ԣ�����Ҫ������Һ�������������Ӧ�����ӷ���ʽΪ��______
��5��������ԭ��Ӧ����������Ӧ�ͻ�ԭ��Ӧ��ɵĶ���ͳһ���磺
3Cu+8HNO3=3Cu��NO��3+2NO��+4H2O?������3Cu-6e-=3Cu2+����ԭ��2NO3-+6e-+8H+=2NO��+4H2O��д����Ͷ������������Һ�з�����Ӧ�����ӷ���ʽ��______���ɲ�ֳ������ͻ�ԭ���̣�������2Al-6e-+8OH-=2AlO2-+4H2O����д��?��ԭ����______��
�ο��𰸣���1����ͬ�����¾����������ʵ���Ҫ����Ϊ���Ĵ�С����1mol��ͬ�������ʵ����������ͬ������������ƽ�������������С�ɺ��ԣ�����ͬ�Ĺ�������С��ͬ������1mol��ͬ�������ʵ����������ͬ����ͬ��ͬѹʱ�κ������һ��������ͬ������ͬ�������������ʵķ��Ӽ�ƽ��������ͬ��
�ʴ�Ϊ�����������ƽ�������������С�ɺ��ԣ�����ͬ�Ĺ�������С��ͬ������1mol��ͬ�������ʵ����������ͬ�����Ӽ��ƽ�����룻
��2��CrԪ����+6�۽���Ϊ+3�ۣ��÷�Ӧ������3molO2ת�Ƶĵ���Ϊ6e-������ת�Ƶķ������Ŀ�������ţ�Ϊ
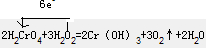
�������ɱ�״��������6.72L��ת�Ƶ��ӵ����ʵ���Ϊ6.72L22.4L/mol��2=0.6mol���ʴ�Ϊ��

��0.6mol��
��3�����������к�����������ӻ�����������ӣ�������������ɻ���Ϊ��ʽ�������Σ�
�ʴ�Ϊ����ʽ�����
��4����H++SO42-+Ba2++OH-=BaSO4��+H2O��֪����ʣ�࣬����Һ�Լ��ԣ���ʹ��ҺΪ����ʱ������������кͷ�Ӧ�����������ӷ�ӦΪH++OH-=H2O��
�ʴ�Ϊ�����ԣ�H++OH-=H2O��
��5����Ͷ������������Һ�з�����Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O=2AlO2-+3H2�����÷�Ӧ��ת�Ƶ���Ϊ6e-��������ӦΪ2Al-6e-+8OH-=2AlO2-+4H2O�����ڱ�֤�����غ�������£������ܵ����ӷ�Ӧ��ȥ������Ӧ�õ���ԭ��ӦΪ6H2O+6e-=3H2+6OH-���ʴ�Ϊ��6H2O+6e-=3H2+6OH-��
���������
�����Ѷȣ�һ��
5��ѡ���� ����������̷������·�Ӧ����2Fe+O2+2H2O=2Fe��OH��2����4Fe��OH��2+O2+2H2O=4Fe��OH��3����2Fe��OH��3=Fe2O3+3H2O������˵����ȷ���ǣ�������
A����Ӧ�١����е���ת����Ŀ���
B����Ӧ�١�����������������
C���١��ڶ����ڵ绯ѧ��ʴ
D��������������ʴ
�ο��𰸣�A����Ӧ��2Fe+O2+2H2O=2Fe��OH��2�е���������O2����Ӧ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��������Ҳ��O2���١���������Ӧ�н���O2���������ҷ�Ӧ����O2������ͬ����ת�Ƶ�������ȣ���A��ȷ��
B����Ӧ�١�������������Ԫ�ػ��ϼ۶����ͣ�������������Ԫ�ػ��ϼ�δ���ͣ�������ֻ����������B��ȷ��
C������������̼���������Ի����Ի����з���������ʴ������ԭ��ط�Ӧ����ӦΪ2Fe+O2+2H2O=2Fe��OH��2����Ϊ�绯��ʴ����4Fe��OH��2+O2+2H2O=4Fe��OH��3Ϊ��ͨ������ԭ��Ӧ����C����
D����Ϊ�绯��ʴ���������μӷ�ӦΪ������ʴ����D��ȷ��
��ѡ��ABD��
���������
�����Ѷȣ���