微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如下所示
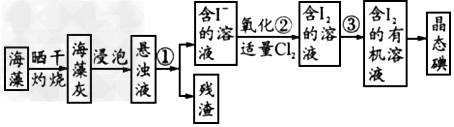
(1)指出从海藻中提取I2的实验操作名称:?①________,③________。②的离子方程式为
__________________。 ?
(2)提取碘的过程中,可供选择的有机溶剂是__________。 ?
A.甲苯、酒精?B.四氯化碳、苯 ?C.汽油、乙酸?D.汽油、甘油 ?
(3)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。尚缺少的仪器是_______________?。 ?
(4)从含碘的有机溶剂中提取碘,还要经过蒸馏,指出图示蒸馏装置中的错误之处_______。

(5)进行蒸馏操作时,使用水浴加热的原因是____________,最后晶态碘在________中。
参考答案:(1)过滤;萃取;2I-+?Cl2=I2+?2Cl-
(2)B?
(3)分液漏斗
(4)①温度计插到了液体中、②冷凝管进出水方向颠倒?
(5)萃取剂沸点较低,I2易升华;烧瓶
本题解析:
本题难度:一般
2、简答题 某固体混合物可能含Al、NH4Cl、MgCl2、Al2(SO4)3、FeCl2中的一种或几种,现对该混合物做如下实验.
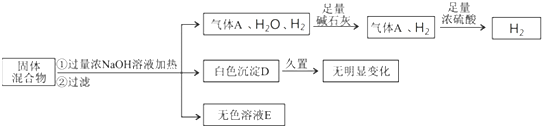
已知气体经过碱石灰和浓硫酸时,二者质量均增大,请回答:
(1)碱石灰的作用是______;气体A是______,生成气体A的离子方程式:______.
(2)写出生成H2的离子方程式是______.
(3)混合物中是否存在FeCl2,理由是______.
(4)白色沉淀D为______(填化学式);固体混合物中不能确定的物质是______(填化学式).
参考答案:(1)碱石灰具有吸水性,可用于吸收气体中的水蒸气;通过碱石灰干燥后再经过浓硫酸,浓硫酸质量增大,说明生成NH3,铵离子与氢氧根离子加热反应生成氨气,反应的离子方程式为:NH4++OH-△.H2O+NH3↑,
故答案为:干燥气体,吸收其中的水蒸气;NH3;NH4++OH-△.H2O+NH3↑;
(2)经过浓硫酸后还剩余气体C,则说明生成H2,一定含有Al,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)白色沉淀D久置无颜色变化,说明含有MgCl2,不含有FeCl2,如生成氢氧化亚铁,会迅速变成灰绿色,最终变成红褐色,
故答案为:白色沉淀D 久置颜色无明显变化,说明不存在FeCl2;
(4)含有MgCl2,生成沉淀为Mg(0H)2,实验过程没有涉及Al2(SO4)3的性质及反应现象,不能确定是否含有Al2(SO4)3,
故答案为:Mg(0H)2;Al2(SO4)3.
本题解析:
本题难度:一般
3、简答题 某化学学习小组的同学设计实验来探究草酸受热分解的产物,他们将草酸受热分解得到的气体通过如下图所示装置:
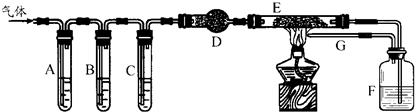
A、C、F中盛装澄清石灰水,B中盛NaOH溶液,E中装有CuO.请填写下列空白:
(1)证明产物中有CO2的现象是______,证明产物中有CO的现象是______.
(2)导管G的作用是______.
(3)小李同学查阅相关资料发现:草酸是二元酸,酸性比碳酸强,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物.小李通过进一步研究认为:草酸蒸气与石灰水反应生成草酸钙白色沉淀,对实验有干扰,因此需要在装置A之前增加一个装有______(填写下列编号字母)的洗气装置.
a.水?b.NaOH溶液?c.Na2CO3溶液?d.饱和NaHCO3溶液
(4)如果在E管中盛装CuO和Cu2O的混合物,根据F瓶增重可以测定混合物中CuO的质量.当CuO和Cu2O的混合物7.6?g全部被还原后,F装置增重3.3?g,混合物中CuO的质量为______?g;当原混合物质量为a?g,反应后F装置增重b?g时,b的取值范围是(用含a的代数式表达)______.
参考答案:(1)草酸受热分解产物中,证明产物中有CO2的现象是装置A中澄清石灰水变浑浊,一氧化碳具有还原性,能将氧化铜还原为金属铜自身被氧化为二氧化碳,如果装置C中澄清石灰水不变浑浊,装置E中黑色固体变为红色,装置F中澄清石灰水变浑浊,可以证明草酸受热分解产物中存在二氧化碳,故答案为:装置A中澄清石灰水变浑浊;装置C中澄清石灰水不变浑浊,装置E中黑色固体变为红色,装置F中澄清石灰水变浑浊;
(2)一氧化碳的尾气处理可以采用点燃法,所以导管G的作用是处理尾气,防止剧毒的CO污染空气,故答案为:处理尾气,防止剧毒的CO污染空气;
(3)草酸分解的气体中含有CO2,用氢氧化钠溶液会将二氧化碳除去,无法进行下一步检验,故b错,草酸既然是酸,那么就会跟碳酸根、碳酸氢根发生反应放出CO2,对检验CO2产生干扰,故c、d错,故选a;
(4)设反应物中CuO为x mol,Cu2O为ymol,混合物7.6g得到产物CO23.3g,根据方程式CuO+CO?△?.?CO2+Cu,
Cu2O+CO?△?.?CO2+2Cu,可列方程组:80x+144y=7.6;(x+y)×44=3.3
? 解得x=0.05,y=0.025,所以CuO质量为:0.05mol×80g/mol=4.0g,根据化学反应,假设原反应物全为CuO,则得CO2为44a80g,假设原反应物全为Cu2O,得CO2为44a144,b的取值范围是:11a36<b<11a20,故答案为:4.0; 11a36<b<11a20.
本题解析:
本题难度:一般
4、选择题 用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
[? ]
A.干燥Cl2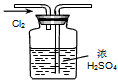
B.吸收HCl 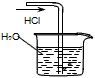
C.石油的分馏 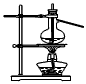
D.吸收NH3
参考答案:D
本题解析:
本题难度:一般
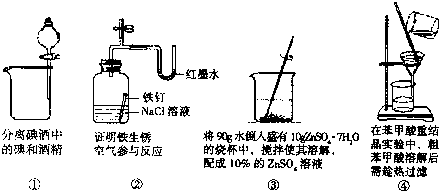
5、简答题 下列装置或操作能达到实验目的是( )
A.①②③④
B.②④
C.②③④
D.①③
参考答案:①碘和酒精混溶,应用蒸馏的方法分离,故①错误;
②铁在NaCl溶液中发生吸氧腐蚀,导致容器内压强降低,U形管左侧液面上升,右侧液面下降,故②正确;
③在90g水中加入10g硫酸锌的结晶水合物,硫酸锌的质量分数小于10%,故③错误;
④苯甲酸溶解度随温度的升高增大,要出气杂质,应趁热过滤,故④正确.
故选B.
本题解析:
本题难度:一般