微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为验证其组成元素,并探究其分子结构进行了下列实验:
(1)验证组成元素将少量样品放入燃烧管A中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置。(夹持仪器的装置已略去)?
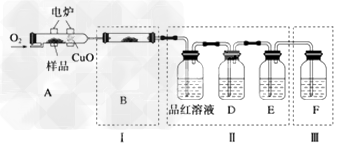
①?写出A中样品燃烧的化学方程式:___________________。
②装置B的目的是验证有机物中含氢元素,则B中盛装的试剂为________。
③D中盛放的试剂是________(填序号)。
a.NaOH溶液b.品红溶液c.酸性KMnO4溶液?d.溴的CCl4溶液e.饱和石灰水
④能证明有机物含碳元素的现象是_________________________。
⑤装置Ⅰ、Ⅱ不能互换的理由是______________________。
⑥燃烧管中放入CuO的作用是____________________。
⑦指出装置F的错误:_____________________。
(2)探究有机物M的分子结构 ?
文献资料表明,该有机物M为二个六元环结构,有很高的对称性,氢原子的环境都相同。将2.04?g该有机物加入溴的CCl4 溶液,充分振荡后溶液褪色,并消耗了0.03?mol?Br2。
⑧该有机物分子结构中含有的官能团为________(填结构式)。
⑨有机物M的结构简式为________(填序号)。
参考答案:(1)①C6H4S4+11O2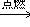 6CO2+4SO2+2H2O
6CO2+4SO2+2H2O
②无水硫酸铜
③c?
④E中溶液不褪色或颜色不变浅,F中溶液变浑浊
⑤气体通过Ⅱ时,会带出水蒸气,干扰氢元素的验证?
⑥将有机物中的碳元素全部氧化成二氧化碳?
⑦试剂瓶未与空气相通?
(2)⑧?
⑨h
本题解析:
本题难度:一般
2、实验题 某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图
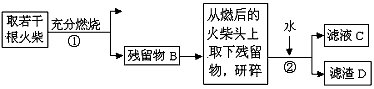
请回答以下问题
(1)为验证气体A,按下图甲所示进行实验:若能观察到__________________的现象,即可证明火柴头上含有S元素。

(2)步骤②的实验操作装置如上图乙所示,该操作的名称是_________________,其工作原理是__________________________。
(3)要证明火柴头中含有Cl元素的后续实验步骤是__________________________。
(4)有学生提出检验火柴头上KClO3另一套实验方案
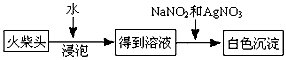
有关的离子反应方程式为_______________________。
(5)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验。
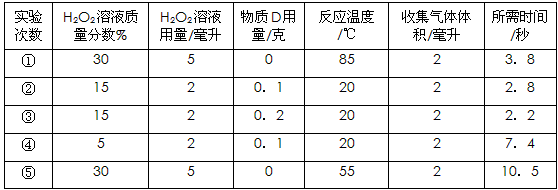
由上表可知,实验①和⑤能证明温度越高,化学反应速率越快,实验_______和_______证明物质D的用量越大,反应速率越快。
(6)写出步骤① 中发生反应的化学方程式__________________________。
参考答案:(1)KMnO4溶液(紫红色)褪色
(2)减压过滤(或抽滤);当打开自来水龙头时,装置内部的空气随自来水被带走,导致装置内部产生负压,从而加快过滤速度,得到较干燥的固体物质
(3)取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素
(4)ClO3-+NO2-+Ag+==AgCl↓+NO3-
(5)②;③
(6)2KClO3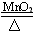 2KCl+3O2↑;S+O2
2KCl+3O2↑;S+O2 SO2
SO2
本题解析:
本题难度:困难
3、选择题 用过量的下列试剂除去粗盐中的CaCl2、MgCl2和Na2SO4杂质,应该最后加入的是( )
A.NaOH
B.BaCl2溶液
C.Na2CO3溶液
D.稀盐酸
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列实验不能达到预期目的的是
[? ]
实验操作 实验目的
A.Cl2、Br2分别与H2反应 比较Cl2、Br2的非金属性强弱
B.Cl2、S分别与Fe反应 比较Cl2、S的氧化性强弱
C.测定相同浓度的Na2CO3、Na2SO4两溶液的pH 比较碳酸、硫酸的稳定性强弱
D.测定相同浓度的盐酸、醋酸两溶液的导电性 比较盐酸、醋酸的酸性强弱?
参考答案:C
本题解析:
本题难度:一般
5、实验题 (Ⅰ)本世纪是生命科学研究的昌盛时期,科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2-),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中
O2-含量,原理是O2-与羟胺反应生成NO2-和一种过氧化物。NO2-在对氨基苯磺酸和α-萘胺作用下,生成粉红的偶氮染体,染体在波长530nm处有显著吸收,且其吸收值与c(NO2-)成正比,从而可计算出样品中的O2-含量。某实验室用以上方法处理后测得溶液中c(NO2-)=2.500×10-3?mol・L-1。
⑴?请根据测定原理写出有关反应的离子方程式________________________;
计算该样品此时c(O2-)?=________________________;?
⑵?如用羟胺氧化法测定O2-时,将其生成的过氧化物作为检测物,若选用氧化还原法进行定量分析(用KMnO4标准溶液进行滴定)
①?请写出其测定原理的反应方程式__________________________;
②?测定所用的主要玻璃仪器为____________,通过观察____________的现象可确定测定反应是否进行完全。
(Ⅱ)水中的NO2-是含氮有机物分解的产物,其浓度的大小是水源污染的标志之一。检测水中的NO2-可用比色法,其步骤是:
a.?配制标准溶液:称取0.30gNaNO2,溶于水后在容量瓶中稀释至1L得溶液A,移取5mL溶液A,稀释至1L,得溶液B。
b.?配制标准色阶:取6只规格为10mL的比色管(即质地、大小、厚薄相同且具塞的平底试管),分别加入体积不等的溶液B,并稀释至10mL,再加入少许(约0.3g)对 苯磺酸粉末,实验结果如下表所示:
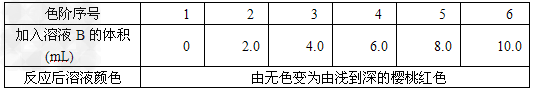
c.?检测:取10mL水样倒入比色管中,加少许对氨基苯磺酸,显色后与标准色阶对比。
请填写以下空白:
①?比色法的基本依据是__________________;
②?若水样显色后与色阶中的5号颜色相同,则表明水样中NO2-含量为___________mg/L。
③?用NaNO2直接配制溶液B的缺点是________________。
④?如果水样显色后比6号还深,应采取的措施是_____________________。
参考答案:(Ⅰ)⑴ NH2OH+2O2-+H+=NO2-+H2O2+H2O;5.000×10-3 mol・L-1;⑵ ① 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;② 酸式滴定管、锥形瓶;锥形瓶中的溶液显浅紫红色
(Ⅱ) ① 溶液颜色的深浅与浓度的大小成正比;② 1.00mg/L;③ 由②计算可知,1L溶液B中只含NO2-1mg,不易称量,直接配溶液B时误差大;④ 将水样先稀释一定倍数后再重复实验
本题解析:
本题难度:一般