微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 在化学研究领域,经常需要对一些物质进行性质的确定。如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下

①准确称量mg金属镁(已除去表面氧化膜),用铜网包住放入干净的试管中;
②按图示组装好装置,然后在关闭活塞的分液漏斗中装入一定体积2mol/L的盐酸;
③调整右边玻璃管(带均匀刻度值),让U型管两端液面在同一水平面,读出右边玻璃管的液面刻度值为V1mL;
④打开分液漏斗活塞,让一定量的盐酸进入试管中后立即关闭活塞;
⑤当镁条反应完后,_______________,读出右边玻璃管的液面刻度为V2mL。
请回答下列问题:
(1)写出你认为步骤⑤中空格应进行的操作。
(2)若V1,V2均是折算为标况下的值,则镁的相对原子质量Ar(Mg)的实验测定表达式为Ar(Mg)=_________,你认为此表达式求出的值是否准确?______(填‘是’或‘不’),主要问题为________________(若回答‘是’则此空不填)。
(3)步骤①中,为什么要用铜网包住镁条?_________________。
参考答案:(1)等装置冷却至室温后,再上下调节右边玻璃管的高度,使两端管内液面在同一水平面
(2)22400m/(V2-V1);不;进入试管中的盐酸的体积也计入了产生的气体体积中
(3)让镁条浸没在盐酸中,防止镁与氧气反应,使镁全部用来产生氢气
本题解析:
本题难度:一般
2、填空题 食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下
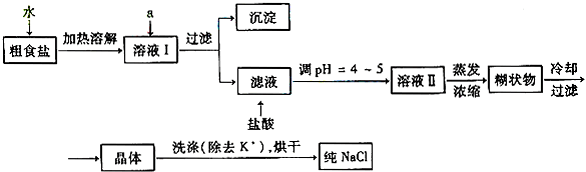
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
① 欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为__________
(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为__________________。
(2)用提纯的NaCl配制500mL4.00 mol・L-1NaCl溶液
① 本次实验所用仪器除药匙、玻璃棒外还有_____________(填仪器称)。
②用托盘天平称取的NaCl晶体的质量为:_____________;
③在配制溶液的过程中多次用到玻璃棒,在溶解时玻璃棒的作用是:_____________, 在移液时玻璃棒的作用是:__________________。
④观察液面时,若俯视刻度线,会使所配制的溶液的浓度_________(填“偏高”、“偏低” 或“无影响”,下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,会__________;
(3)用ρ=1.84g・mL-1,质量分数为98%的浓硫酸配制200mL1mol・L-1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V=___________mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用_____________(填仪器名称)。
③溶解:稀释浓硫酸的方法_________________________________________。
参考答案:(1)①BaCl2、NaOH、Na2CO3;②75%乙醇
(2)①天平、烧杯、500mL容量瓶、胶头滴管;②117.0g;③搅拌加速溶解;引流;④偏高;偏低
(3)①10.87;②酸式滴定管;③将浓硫酸沿器壁慢慢注入水中,并不断搅拌,使稀释产生的热量及时散出
本题解析:
本题难度:一般
3、选择题 下列装置或操作不能达到实验目的的是
[? ]
A. 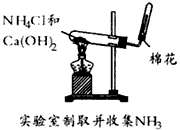
B. 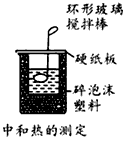
C. 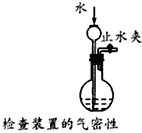
D. 
参考答案:B
本题解析:
本题难度:一般
4、实验题 (三选一)【化学与技术】
以食盐为原料进行生产并综合利用的某些过程如图所示。

(1)除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是________(填序号)。
a.Na2CO3 ?b.NaOH? c.BaCl2
(2)将滤液的pH调至酸性除去的离子是____________。
(3)电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是_________________。
(5)某探究活动小组将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。

试回答下列有关问题:
①乙装置中的试剂是________;
②丁装置中稀硫酸的作用是________;
③实验结束后,分离出NaHCO3晶体的操作是____(填分离操作的名称)。
(6)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污,其原因是_______________(结合离子方程式表述)。
②工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是______。(已知碳酸的酸性强于次氯酸)
参考答案:(1)cab(或cba或bca)
(2)CO32-和OH-
(3)NaCl+H2O NaClO+H2↑
NaClO+H2↑
(4)NH3
(5)①饱和碳酸氢钠溶液;②吸收未反应的NH3;③过滤
(6)①CO32-水解显碱性:CO32-+H2O HCO3-+OH-,油污在碱性条件下水解,能达到去污目的;②2CO32-+Cl2+H2O= Cl-+ClO-+2HCO3-
HCO3-+OH-,油污在碱性条件下水解,能达到去污目的;②2CO32-+Cl2+H2O= Cl-+ClO-+2HCO3-
本题解析:
本题难度:一般
5、选择题 下列有关实验原理,方法和结论都正确的是( )
A.某钠盐溶液中加入硝酸无明显现象,再加入氯化钡溶液有白色沉淀,该钠盐一定是硫酸钠
B.在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
C.新制氯水中加入碳酸钙粉末搅拌,过滤、滤液中c(HClO)将增大
D.相同质量的两份锌粒分别加入足量稀硫酸,在一份中加入少量CuSO4?5H2O,其反应速率将加快,且最终产生的H2与另一份相同
参考答案:C
本题解析:
本题难度:一般