��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵���������
[? ]
A����ѧ��Ӧ�е������仯ͨ������Ϊ�����ı仯
B����ѧ���Ķ��Ѻ��γ��ǻ�ѧ��Ӧ�������仯����Ҫԭ��
C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D����Ӧ��������������������������Դ�С�����˷�Ӧ�Ƿų�����������������
�ο��𰸣�C
���������
�����Ѷȣ���
2������� (10��)2007��ŵ������ѧ������߸���¡����ض������˺ϳɰ���Ӧ���ơ�T=673Kʱ��������Ӧ�������仯��ͼ��ʾ��ͼ�е�������λΪkJ��mol-1��ע��ͼ�С�������ʾ�ڴ������������������ش��������⣺
��1���ϳɰ���Ӧ�Ļ���Ϊ
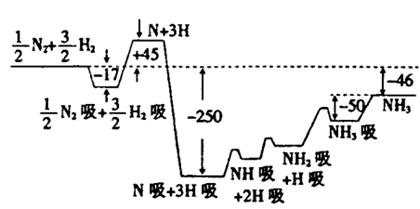
��?
��N2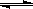 N2��
N2��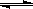 ?2N
?2N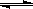 2N��
2N��
��N��+H��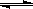 NH��
NH��
��NH��+H��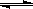 NH2��
NH2��
��NH2��+H��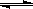 NH3��
NH3��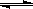 NH3
NH3
��2��T=673K���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ?��
��3��Һ����ˮ��Ϊ���������ܽ���������л����ӣ�����뷽��ʽ�ɱ�ʾΪ2NH3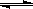
 +
+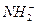 ��ij�¶��������ӻ�����Ϊ10-30����Һ���е�pNH4��ˮ�е�pH���ƣ�����¶���Һ����pNH4=_________________��
��ij�¶��������ӻ�����Ϊ10-30����Һ���е�pNH4��ˮ�е�pH���ƣ�����¶���Һ����pNH4=_________________��
��4�������£�N2H6Cl2����һ����Ҫ�Ļ���ԭ�ϣ��������ӻ������������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�д�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽ_________________��
�ο��𰸣���1����H2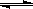 H2��
H2��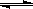 2H
2H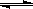 2H����2�֣�
2H����2�֣�
��2��N2��g��+3H2��g��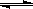 2NH3��g����H=-92kJ��mol-1��3�֣�
2NH3��g����H=-92kJ��mol-1��3�֣�
��3��15��3�֣�
��4��N2H62++H2O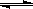 [N2H5��H2O]++H+��2�֣�
[N2H5��H2O]++H+��2�֣�
�����������
�����Ѷȣ���
3��ѡ���� ���б仯�����У���Ҫ���ȵ���(? )
A����ʯ����ˮ���
B����Ȼ��ȼ��
C��Ũ��������ˮ
D���ɱ�����
�ο��𰸣�D
���������A��B��C���Ƿ��ȵģ��ɱ�������Ҫ���ȣ���ѡD��
��������Ҫ���Ȼ���ȵĹ��̲�һ�������ȷ�Ӧ����ȷ�Ӧ����Ϊֻ���ڻ�ѧ��Ӧ�в��ַܷ��ȷ�Ӧ�����ȷ�Ӧ��
�����Ѷȣ���
4��ѡ���� ��NA���������ӵ�������������Ȼ�ѧ����ʽC2H2��g��+
O2��g���T2CO2��g��+H2O��l����H=-1300kJ?mol-1��˵���У���ȷ���ǣ�������
A��10NA������ת��ʱ���÷�Ӧ�ų�1300kJ������
B��NA��ˮ����������ΪҺ��ʱ������1300kJ������
C����2NA��̼�����õ��Ӷ�����ʱ���ų�1300kJ������
D����10NA��̼�����õ��Ӷ�����ʱ���ų�1300kJ������
�ο��𰸣�A��10NA�����ӵ����ʵ���Ϊ10mol����Ӧ��̼Ԫ�صĻ��ϼ���-1������Ϊ+4���μӷ�Ӧ����Ȳ�����ʵ���Ϊ10mol2��5=1mol���ų�������Ϊ1300kJ/mol��1mol=1300kJ����A��ȷ��
B���Ȼ�ѧ����ʽ�С�H��0��ʾ���ȣ�C2H2��g��+52O2��g��=2CO2��g��+H2O��l����H=-1300kJ/mol�÷�ӦΪ���ȷ�Ӧ����NA��ˮ����������ΪҺ��ʱ���ų�1300kJ����������B����
C��1��CO2�����к���4�����õ��Ӷԣ���8NA��̼�����õ��Ӷ�����ʱ��˵����2molCO2���ɣ��ų�1300KJ����������2NA��̼�����õ��Ӷ�����ʱ��˵����0.5molCO2���ɣ��ų�1300KJ4=325KJ����������C����
D��1��CO2�����к���4�����õ��Ӷԣ���10NA��̼�����õ��Ӷ�����ʱ��˵����2.5molCO2���ɣ��ų�������Ϊ1300KJ��2.52=1625KJ����D����
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� ���б仯���̣����ڷ��ȷ�Ӧ���� (? )
����ʯ����ˮ��Ӧ����NH4Cl������Ba(OH)2��8H2O��Ͻ��裻�۴�����룻�ܹ���������������ˮ����H2��Cl2��ȼ�գ���ŨH2SO4ϡ�ͣ�������кͷ�Ӧ
A���٢ڢ�
B���٢ݢ�
C���٢ܢݢޢ�
D���ۢޢ�
�ο��𰸣�B
�������������ʯ����ˮ��ӦΪ���ȷ�Ӧ����NH4Cl������Ba(OH)2��8H2O��Ͻ���Ϊ���ȷ�Ӧ���۴������Ϊ���ȹ��̣����ǻ�ѧ��Ӧ���ܹ���������������ˮ�����ǻ�ѧ��Ӧ���Ƿ��ȹ��̣��� ŨH2SO4ϡ�ͣ��Ƿ��ȹ��̣����ǻ�ѧ�仯����B��ȷ��
�����Ѷȣ�һ��