微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)一种“人工固氮”的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和氧气。已知:
化学键
| N≡N
| H―O
| N―H
| O=O
|
键能/kJ・mol-1
| 945
| 463
| 391
| 498
|
(1)请根据以上信息,写出“人工固氮”新方法的热化学方程式:_____▲______;
(2)进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
T/℃
| 30
| 40
| 50
|
生成NH3量/(10-6mo1/L)
| 4.8
| 5.9
| 6.0
|
①50℃时从开始到3 h内以O2物质的量浓度变化表示的平均反应速率为? ▲?;
②与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议(请写出两条)? ▲?、? ▲?;
(3)氨是氮肥工业的重要原料。某化肥厂生产铵态氮肥(NH4)2SO4的工业流程如下:
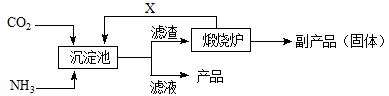
①往沉淀池中装入CaSO4悬浊液后,需先通入足量NH3,再通入CO2的原因是
? ▲?。
②煅烧炉中产生的固态副产品为? ▲?,生产流程中能被循环利用的物质X为? ▲?。
参考答案:(14分)
(1)N2(g) + 3H2O( g) 2NH3(g) +
2NH3(g) + 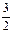 O2(g);△H =" +" 630 kJ・mol-1?(3分)
O2(g);△H =" +" 630 kJ・mol-1?(3分)
(2)①2.5×l0-8 mol/(L・min)或①1.5×l0-6 mol/(L・h)?(2分)
②升高温度;增大压强;?(合理均可,2分)
(3)①氨在水中溶解度大,使溶液呈碱性,有利于吸收CO2,增大c(CO32-),促使CaSO4转化为CaCO3,同时生成(NH4)2SO4?(3分)
②CaO(或生石灰)? CO2(或二氧化碳)?(各2分,共4分)
本题解析:略
本题难度:一般
2、实验题 我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:
NH3+CO2+H2 O
O ??NH4HCO3;? NH4HCO3+NaCl ??NaHCO3↓+NH4Cl ;
2NaHCO3 Na2CO3
Na2CO3 +CO2↑+H2O
+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是?(填字母标号);
a.碳酸氢钠难溶于水?
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小, 所以在溶液中首先结晶析出
所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制 碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如右图所示(图中夹持、固定用的仪器未画出)。
试回答下列有关问题:
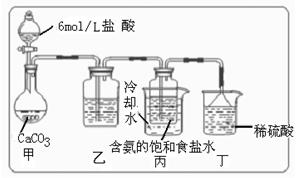
 (Ⅰ)乙装置中的试剂是?
(Ⅰ)乙装置中的试剂是? ?
?
(Ⅱ)丁装置中稀硫酸的作用是?
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是?(填分离操作的名称)。
(IV)请你再写出一种实验室制取少量碳酸氢钠的方法:?。
参考答案:(1)C?
(2)(Ⅰ)饱和碳酸氢钠溶液
(Ⅱ)吸收未反应的NH3(答“防止倒吸”或“吸收CO2”不给分)?
(Ⅲ)过滤
(IV)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2;往饱和Na2CO3溶液中通入过量CO2等。其他合理方法均可)
本题解析:略
本题难度:简单
3、实验题 (10分)氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如下所示,完成下列填空:
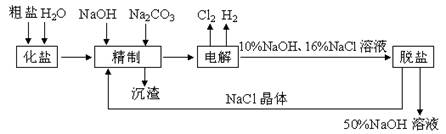
(1)在电解过程中,与电源正极相连的电极上电极反应为__________________,与电源负极相连的电极附近,溶液pH_________(选填“不变”、“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为_________
_______________________________________________________________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是_________。
a. Ba(OH)2? b. Ba(NO3)2? c. BaCl2
(4)为了有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_________(选填a、b、c)
a. 先加NaOH,后加Na2CO3,再加钡试剂?
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过_________、冷却、_________(填写操作名称)除去NaCl。
参考答案:(1)2Cl--2e-="=" Cl2↑?(1分) ?升高(1分)
(2)Ca2++CO32-="=" CaCO3 ↓?(1分)? Mg2++2OH-="=" Mg(OH)2↓?(1分)
(3)ac(2分)?(4)bc(2分)
(5)加热蒸发?(1分)?过滤(1分)
本题解析:略
本题难度:一般
4、选择题 下列气体中,能用98.3%的浓硫酸干燥的是( )
A.SO3(气)
B.SO2
C.H2S
D.NH3
参考答案:B?
本题解析:SO3气体易溶于浓H2SO4中,H2S易被浓H2SO4氧化,NH3显碱性,不能用浓H2SO4干燥。
本题难度:简单
5、填空题 “绿色化学”要求利用化学原理从源头消除污染,减少或消除在化工产品的设计、生产及应用中有害物质的使用和产生。“绿色化学”要求化学反应和化学工业过程以“原子经济性”为基本原则,在获取新物质的化学反应中充分利用参与反应的原料的每一个原子,实现“零排放”。
(1)下列化学反应符合绿色化学概念的是________。
A.制取有机玻璃的单体: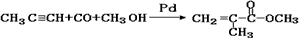
B.制取CuSO4: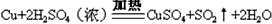
C.制取乙苯: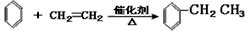 (催化剂是氯化铝,氯化铝和加入的盐酸都有较强的腐蚀性,生产过程中产生大量废液、废气)
(催化剂是氯化铝,氯化铝和加入的盐酸都有较强的腐蚀性,生产过程中产生大量废液、废气)
D.制取Cu(NO3)2:2Cu+O2 2CuO? CuO+2HNO3(稀)=Cu(NO3)2+H2O
2CuO? CuO+2HNO3(稀)=Cu(NO3)2+H2O
(2)化学电池在通讯、交通及日常生活中有着广泛的应用。但废旧电池的妥善处理已成为我们日常生活十分头痛的问题,资料表明一节废镍锡电池可以使一平方米面积的耕地失去使用价值。常用的镍镉电池的总反应可以表示为:Cd+2NiO(OH)+2H2O 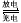 2Ni(OH)2+Cd(OH)2 已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。在酸性土壤中这种污染尤为严重。这是因为_______________________。
2Ni(OH)2+Cd(OH)2 已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。在酸性土壤中这种污染尤为严重。这是因为_______________________。
(3)硫酸工业的尾气中主要含有气体,下列有关它的叙述错误的是________。
A.形成硫酸型酸雨
B. 破坏臭氧层
C. 不会腐蚀建筑物
D.能跟血红蛋白结合使人体中毒
E.能使品红、酸性KMnO4褪色,并且褪色原理相同
该尾气我们可采用过量氨水吸收,请写出化学反应方程式________________。请判断这种处理方法是否符合绿色化学的概念___(填“是”或“否”)并说明理由__________________。
参考答案:(1)A D
(2)在酸性土壤中Ni(OH)2和Cd(OH)2都与酸反应,溶解生成了Ni2+、Cd2+,对土壤和水体的污染更严重。
(3)DE;SO2 + 2NH3・H2O=(NH4)2SO3;是;(NH4)2SO3可以继续被氧化生成硫酸铵,而硫酸铵是一种常用的氮肥,既吸收了尾气,又生成了一种有使用价值的化肥。
本题解析:
本题难度:一般