微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
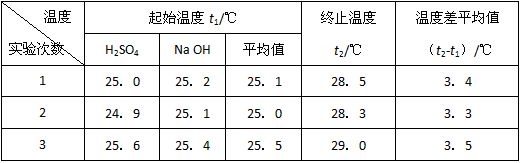
1、实验题 利用下图装置测定中和热的实验步骤如下:

①量取50mL 0.25 mol/L硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。
请回答:
(1)NaOH溶液稍过量的原因 ____________。
(2)加入NaOH溶液的正确操作是_____________ (填字母)。
A.沿玻璃棒缓慢加入
B.一次迅速加入
C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是__________ 。
(4)设溶液的密度均为1g・cm-3,中和后溶液的比热容c=4.18 J・(g・℃)-1,
请根据实验数据写出该反应的热化学方程式_____________ 。
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量__________ (填“小于”、“等于”或“大于”)57.3 kJ,原因是________________ 。
参考答案:(1)确保硫酸被完全中和
(2)B
(3)用环形玻璃棒轻轻搅动
(4)H2SO4(aq)+2NaOH(aq)== Na2SO4(aq)+2H2O(l);ΔH=-113.6kJ・mol-1
(5)大于; 浓硫酸溶于水放出热量
本题解析:
本题难度:一般
2、选择题 如图所示的实验装置或操作不能达到实验目的是( ? )
A.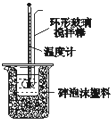
测定中和反应的反应热
B.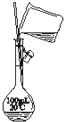
配制100mL 0.1mol/L盐酸
C.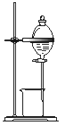
用来分离乙醇和水
D.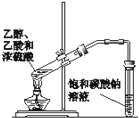
实验室制备乙酸乙酯
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列实验操作中,错误的是
[? ]
A.配制100 g 5%的食盐溶液时,需将5 g食盐放入烧杯中,加95 mL水搅拌溶解即可
B.配制0.1 mol・L-1的硫酸溶液时,将量取的浓硫酸放入容量瓶中加水稀释
C.测定硫酸铜晶体结晶水含量时,需边加热边搅拌,防止晶体飞溅
D.中和热测定实验中,应用环形玻璃搅拌棒轻轻搅动混合液
参考答案:B
本题解析:
本题难度:简单
4、选择题 强酸和强碱的稀溶液发生中和反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ・mol-1分别向1 L 0.5 mol・L-1的NaOH溶液中加入:稀醋酸、浓硫酸、稀硝酸,则恰好完全反应时的热效应ΔH1、ΔH2、ΔH3的关系正确的是
A.ΔH1>ΔH3>ΔH2
B.ΔH2>ΔH3>ΔH1
C.ΔH2=ΔH3>ΔH1
D.ΔH1=ΔH2=ΔH3
参考答案:A
本题解析:
本题难度:困难
5、简答题 中和热的测定实验(如图).
①量取反应物时,取50mL0.50mol?L-1的盐酸,还应加入的试剂是______(填序号).
A.50mL0.50mol?L-1NaOH溶液
B.50mL0.55mol?L-1NaOH溶液
C.1.0gNaOH固体
②在该实验过程中,该同学需要测定的实验数据有______(填序号).
A.盐酸的浓度 B.盐酸的温度
C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度
E.水的比热容 F.反应后混合溶液的终止温度
③若用50mL0.5mol?L-1醋酸溶液代替上述盐酸测定中和热,所得数据______.(填“偏大”或“偏小”或“不变”)
参考答案:①为了保证酸或是碱中的一方完全反应,往往保证一方过量,所以可以选择50mL 0.55mol?L-1 NaOH溶液,故答案为:B;
②在该实验过程中,该同学需要测定的实验数据有酸、碱的初始温度以及反应后混合溶液的终止温度,故答案为:BDF;
③醋酸为弱酸,电离过程为吸热过程,所以醋酸(CH3COOH)代替HCl溶液反应,反应放出偏小,故答案为:偏小.
本题解析:
本题难度:一般