��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
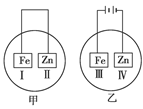
1��ѡ���� ����Ƭ��пƬ����ʢ��NaCl��Һ(���е��з�̪)�ı������У�����ͼ��ʾ�����ȹ۲쵽��Ϊ��ɫ������Ϊ(����)
A����͢�
B����͢�
C����͢�
D����͢�
�ο��𰸣�B
�����������ͼʾ��ԭ��أ�п��������пʧ�����γ�п���ӣ������Ǣ��������ϣ�O2+2H2O+4e-=4OH-�����Ԣ�죻��ͼʾ�ǵ��أ�������������ʧ���������������ӣ�п���������������ϣ�2H++2e-=H2�����ƻ���пƬ����ˮ�ĵ���ƽ�⣬ʹ��OH-Ũ���������Ԣ���Ҳ��죮��ѡB��
���������⿼����ԭ��غ͵��صĹ���ԭ����Ӧ�ã���Ҫ�ǵ�ⷴӦ�����ӱ仯��
�����Ѷȣ���
2������� ij����С��ֱ�����ͼ��ʾװ�ö�ԭ��غ͵��ԭ������ʵ��̽����
��ش�
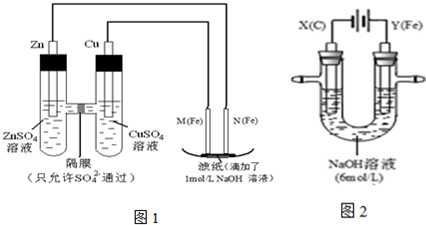
I����ͼ1��ʾװ�ý��е�һ��ʵ�飮
��1���ڱ�֤�缫��Ӧ���������£��������Cu���缫����______������ĸ��ţ���
A������������?B��ʯī��������?C����������?D����
��2��N��������Ӧ�ĵ缫��ӦʽΪ______��
��3��ʵ������У�SO42-______����������ҡ������������������ƶ�����ֽ���ܹ۲쵽��������______��
II����ͼ2��ʾװ�ý��еڶ���ʵ�飮ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���壮�������Ϸ��֣����������FeO42-������Һ�г��Ϻ�ɫ��
��4���������У�X������Һ��pH______�����������С�����䡱����
��5���������У�Y�������ĵ缫��ӦΪFe-6e-+8OH-�TFeO42-+4H2O��______��
��6������X���ռ���672mL���壬��Y���ռ���168mL���壨��������Ϊ��״��ʱ�������������Y�缫�����缫����������______��g��
��7���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn�TFe2O3+ZnO+2K2ZnO2���õ�����������ķ�Ӧ�ĵ缫��ӦʽΪ______��
�ο��𰸣���1���ڱ�֤�缫��Ӧ���������£���Ȼ��п�����������������ϱ����Dz���п���õĽ�����ķǽ��������DZ�п���õĽ��������Բ��ܴ���ͭ����ѡA��
��2��N�缫����ԭ��ظ����������ǵ��������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ��2H++2e-�TH2������2H2O+2e-�TH2��+2OH-�����ʴ�Ϊ��2H++2e-�TH2������2H2O+2e-�TH2��+2OH-����
��3��ԭ��طŵ�ʱ�����������ƶ���������������������ƶ��������У������������ӵõ���������������������ʧ���������������ӣ��������Ӻ����������ӷ�Ӧ��������������������������������������������������������ֽ���к��ɫ�ߵ�������ʴ�Ϊ������������ֽ���к��ɫ�ߵ������
��4���������У������������ӷŵ�������������������������������Ũ�ȴ�����������Һ����Һ�ʼ��ԣ���Һ��pH���ʴ�Ϊ����
��5�����ǻ��ý��������ع���ʱ����������ʧ���ӷ���������Ӧ������������ʧ���ӷ���������Ӧ�����Է����ĵ缫��ӦʽΪ��Fe-6e-+8OH-�TFeO42-+4H2O��4OH--4e-�T2H2O+O2����
�ʴ�Ϊ��4OH--4e-�T2H2O+O2����
��6��X�缫����������������Y�缫������������������Y�缫ʧ���ӽ�����Һ��������������Ϊxg������ת�Ƶ�������ȵ�0.672L22.4L/mol��2=0.168L22.4L��4+xg56g/mol��6��x=0.28��������������0.28g��
��7�������ϸ���������ӵõ��ӷ�����ԭ��Ӧ����Ӧ����ʽΪ2FeO42-+6e-+5H2O�TFe2O3+10OH-��
�ʴ�Ϊ��2FeO42-+6e-+5H2O�TFe2O3+10OH-��
���������
�����Ѷȣ�һ��
3��ѡ���� ���õ�ť��ʽ��п��أ��ŵ�ʱ�ĵ缫��Ӧʽ�ֱ�Ϊ��
Zn����Zn+2OH-+2e- = Zn(OH)2 ?Ag2O����Ag2O+H2O+2e- =2Ag+2OH-������˵���в���ȷ���ǣ�?��
A���ŵ������[OH-]����
B��Zn������Ag2O����
C���������Һ�ʼ���
D�����Ӵ�Ag2O�������õ�������Zn��
�ο��𰸣�D
������������ݵ缫��Ӧʽ���жϣ�пʧȥ���ӣ�����п�Ǹ������������õ����ӣ������������B��ȷ��D����ȷ���ܵķ�Ӧʽ��Zn��Ag2O��H2O��Zn(OH)2 ��2Ag������A��C������ȷ�ģ���ѡD��
�����������Ǹ߿��еij������ͣ�Ϊ�е��Ѷȵ����⡣��Ҫ��ѵ��ѧ���������֪ʶ���������������������ɡ��ܽ������������
�����Ѷȣ���
4������� ��ͼ��ʾ�����һ��ԭ��أ��Իش��������⣨���ݹ��ʺ��ʣ���
��1���������ҺΪϡH2SO4ʱ������______����������������������a�⣬���������b�⣩��
a��������������Mg�缫�Ϸ����ķ�ӦΪ��______��Al�缫�Ϸ����ķ�ӦΪ��______��
b�������ݲ�����������Ϊ����
��2���������ҺΪNaOH��aq��ʱ������______����������������������a�⣬���������b�⣩��
a��������������Mg�缫�Ϸ����ķ�ӦΪ��______��Al�缫�Ϸ����ķ�ӦΪ��______��
b�������ݲ�����������Ϊ����
�ο��𰸣���1������þ����Ϊ�缫���ϣ��������ҺΪϡH2SO4ʱ�����γ�ԭ��أ�����þ�������ã���ԭ��صĸ���������ԭ��ص�������������ӦΪMg-2e-=Mg2+��
������ӦΪ2H++2e-=H2������ʱ���ݱ������ʴ�Ϊ������Mg-2e-=Mg2+��2H++2e-=H2����
��2������þ����Ϊ�缫���ϣ��������ҺΪϡNaOHʱ�����ڽ�������������������Һ��Ӧ����ƫ��������Һ��������������Ϊ������þΪ������
������ӦΪ2Al-6e-+8OH-=2AlO2+4H2O��������ӦΪ6H2O+6e-=3H2+6OH-���γ�ԭ���ʱ�����ݱ�����
�ʴ�Ϊ������6H2O+6e-=3H2+6OH-��2Al-6e-+8OH-=2AlO2+4H2O��
���������
�����Ѷȣ�һ��
5������� ��ʵ�����п�������ͼ��ʾװ��ģ������ȼ�ϵ�صĹ���ԭ����a��b���缫Ϊ���̼������
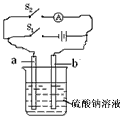
��1�����Ͽ���S1����ͨ��Դ�����Լ����ӣ��������缫�Ϲ۲쵽��������______________________����缫a��________���������ĵ缫��ӦΪ________________________��
��2��Ȼ���S1������S2����ʱ��������ָ�뷢��ƫת�����װ����a����Ϊ_____________________��
�ο��𰸣���1����̼���������ݲ���������2H++2e-=H2��
��2����
���������
�����Ѷȣ�һ��