��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �йآ�100ml?0.1?mol/L?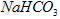 ����100ml?0.1?mol/L?
����100ml?0.1?mol/L?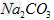 ������Һ����������ȷ����?
������Һ����������ȷ����?
[? ]
A.��Һ��ˮ������� ��������>��?
��������>��?
B.��Һ�������ӵ����ʵ���Ũ��֮��:��>��
C.����Һ��:?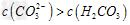 ?
?
D.����Һ��:?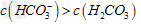
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� �������ʵ���Ũ�ȡ���������������ռ���Һ��Ϻ�����ɫʯ����Һ����Һ��
A.��ɫ
B.��ɫ
C.��ɫ
D.��ɫ
�ο��𰸣�B
�����������������������ʵ���������NaOH��Ϻ�H+���������ɵ���������Һ�����ԣ����Է�Ӧ�����Һ�еμ�ʯ����Һ�ʺ�ɫ��
���㣺��ѧ����
�������������������Ʒ�Ӧ�����ӷ���ʽΪH++OH-=H2O�������ʵ���H2SO4��NaOH��Ӧ��H+������
�����Ѷȣ�����
3������� ������ˮ��Һ�е���Ϊ����ѧ��ѧ����Ҫ���ݣ���֪�������ʵĵ��볣��ֵ��25�棩��
HClO��Ka=3��10-8��HCN��Ka=4.9��10-10
H2CO3��Ka1=4.3��10-7��Ka2=5.6��10-11
��1��84����Һ��ͨ��������CO2���÷�Ӧ�Ļ�ѧ����ʽΪ______��
��2��25��ʱ�������ʵ���Ũ�ȵĢ�NaClO��Һ����Na2CO3��Һ����NaCN��Һ������Һ��pH�ɴ�С��˳��Ϊ______������ţ���
��3�������ʵ���NaClO��NaHCO3�Ļ��Һ�У�����Ũ�ȵĹ�ϵΪ��[Na+]=______+[H2CO3]
��4��ʵ���ҿ�����ͼ��ʾװ���Ʊ�84����Һ����aΪ______�����Ʊ��������ܵ����ӷ�Ӧ����ʽΪ______��
��5��25��ʱx?mol?L-1CH3COOH��Һ��0.01mol?L-1?NaOH��Һ�������ϣ���Һ�����ԣ���[CH3COO-]______[Na+]��ѡ���������������=�������ú�x�Ĵ���ʽ��ʾCH3COOH�ĵ���ƽ�ⳣ��Ka=______��
�ο��𰸣���1����Ka��֪̼������ԣ�HClO����84����Һ��ͨ��������CO2�ķ�ӦΪNaClO+CO2+H2O�THClO+NaHCO3��
�ʴ�Ϊ��NaClO+CO2+H2O�THClO+NaHCO3��
��2�������ʵ���Ũ�ȵ�����Һ����Խ�������Ӧ�ε�ˮ��̶�Խ��pH��Խ����Ka��֪������HClO��HCN��HCO3-��������ʵ���Ũ�ȵĢ�NaClO��Һ����Na2CO3��Һ����NaCN��Һ������Һ��pH�ɴ�С��˳��Ϊ�ڣ��ۣ��٣��ʴ�Ϊ���ڣ��ۣ��٣�
��3�������ʵ���NaClO��NaHCO3�Ļ��Һ�У��������غ��֪��n��Na��=n��Cl��+n��C������[Na+]=[ClO-]+[HClO]+[HCO3-]+[HCO32-]+[H2CO3]��
�ʴ�Ϊ��[Na+]=[ClO-]+[HClO]+[HCO3-]+[HCO32-]��
��4����ͼ��֪��aΪ������bΪ���������¶������ӷŵ��������������϶����ɵ�NaOH��Һ��Ӧ����NaClO�������ӷ�ӦΪCl-+H2O?���?.?ClO-+H2����
�ʴ�Ϊ������Cl-+H2O?���?.?ClO-+H2����
��5�����ݵ���غ�ʽΪ[CH3COO-]+[OH-]=[Na+]+[H+]����Һ������ʱ[OH-]=[H+]����[CH3COO-]=[Na+]���ֵ���ƽ�ⳣ��Ka=c(CH3COO-)c(H+)c(CH3COOH)��c��H+��=10-7mol/L��[CH3COO-]=[Na+]=0.005mol/L��c��CH3COOH��=x2mol/L����Ka=10-9x-10-2���ʴ�Ϊ��=10-9x-10-2��
���������
�����Ѷȣ�һ��
4��ѡ���� ���������ʣ���H2SO4����CO2����NaOH����BaSO4����NH3����SO2����NH3?H2O����C2H5OH����Cu�����Ȼ�����Һ��Ҫ������ȷ���ǣ�������
A��������ʣ��ܡ���
B������ʣ��١��ۡ��ܡ���
C���ǵ���ʣ��ڡ��ݡ��ޡ���
D��ǿ����ʣ��١��ۡ���
�ο��𰸣�����H2SO4��ˮ��Һ�����ȫ����������ƶ��������Ӻ���������ӵ��µ��磬����H2SO4��ǿ����ʣ�
��CO2��ˮ��Һ�����̼�ᣬ̼���ܵ���������ƶ��������Ӻ�̼������ӵ��µ��磬���Ƕ�����̼�������룬���Զ�����̼�Ƿǵ���ʣ�
��NaOH��ˮ��Һ���������״̬�£�����ȫ����������ƶ��������Ӻ����������ӵ��µ��磬����NaOH��ǿ����ʣ�
��BaSO4�����Σ�����ˮ�IJ��ֻ�������״̬ʱ��������ȫ���������ӣ�����ǿ����ʣ�
��NH3����ˮ���ܺ�ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ��ܵ���������ƶ����������ӣ���������������ӵ���һˮ�ϰ�������NH3������NH3�Ƿǵ���ʣ�
��SO2Ϊ�������ˮ��Һ�ܵ��磬���䱾�����������룬�����ڷǵ���ʣ�
��NH3?H2O��ˮ��Һ�в�����ȫ���룬NH3?H2O�������������ʣ�
��C2H5OH��ˮ��Һ�������Ҵ����ӵ���ʽ���ڣ����Բ����磬����Ϊ�ǵ���ʣ�
��Cu�ܵ��磬�ǵ��ʣ����Ȳ��ǵ���ʣ�Ҳ���Ƿǵ���ʣ�
���Ȼ�����Һ�ܵ���������ƶ��������Ӻ������ӣ��ܵ��磬�����ǻ������Ȳ��ǵ���ʣ�Ҳ���Ƿǵ���ʣ�
A����BaSO4����ǿ����ʣ���NH3?H2O��������ʣ���A����
B����H2SO4��NaOH����BaSO4��NH3?H2O�ǵ���ʣ���B��ȷ��
C����CO2��NH3����SO2��C2H5OH�Ƿǵ���ʣ���C��ȷ��
D����H2SO4��NaOH��BaSO4��ǿ����ʣ���D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� ��������������У�����֤������������ʵ���
A.1 mol��L-1������Һ��pHֵԼΪ2
B.����������������ȫ����H+
C.10 mL1 mol��L-1������10 mL1 mol��L-1NaOH��Һ��ȫ��Ӧ����Һ�ʼ���
D.��[H+]1 mol��L-1������Һ100 mL������Zn��Ӧ�ų���״����H2���������1.12 L
�ο��𰸣�B
���������
�����Ѷȣ���