��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ȷ����(����)
A�����ô����ܽ⺬̼��Ƶ�ˮ����CaCO3��2H��=Ca2����H2O��CO2��
B����ͭΪ�缫��ⱥ��ʳ��ˮ��2Cl����2H2O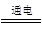 Cl2����H2����2OH��
Cl2����H2����2OH��
C����������Һ�еμӹ�����ˮ��Al3����4NH3��H2O=AlO2����4NH4+��2H2O
D����С�մ���Һ�м�����Ba(OH)2��Һ��2HCO3����Ba2����2OH��=BaCO3����2H2O��CO32��
�ο��𰸣�D
���������A���д���ӦдΪ��ѧʽ��B����ͭΪ�缫���ʱͭ���뷴Ӧ��C����Al(OH)3�����ܽ��ڰ�ˮ�С�
�����Ѷȣ�һ��
2������� ��Ҫ��ȷ�������б仯�����еĻ�ѧ������У�1��~��3��д��ѧ����ʽ����4��~��5��д���ӷ���ʽ��
��1����˿��������ȼ��?�� ��2��������SO2������?��
��3��þ�ڶ�����̼��ȼ��?����4��NaOH��Һ��NaHCO3��Һ��Ӧ?��??
��5�����Ȼ�����Һ�̻���·��?��
�ο��𰸣���1��3Cl2 +2Fe 2FeCl3?��2��SO2+2H2S=3S+2H2O?��3��2Mg+CO2
2FeCl3?��2��SO2+2H2S=3S+2H2O?��3��2Mg+CO2 2MgO+C
2MgO+C
��4��OH-+HCO3-= CO32-+H2O?��5��) 2Fe3++Cu��2Fe2++Cu2+
�����������1��������ǿ�������ԣ����ѱ�۽���Fe��Cu�������γɸ�̬�����ʡ���˿��������ȼ�յĻ�ѧ����ʽΪ3Cl2 +2Fe 2FeCl3����2��SO2���������ԣ����л�ԭ�ԣ��仹ԭ�Խ�ǿ�������Խ���������SO2+2H2S=3S+2H2O����3��þ����������������ȼ�գ�Ҳ�����ڶ�����̼��ȼ�գ���Ӧ�Ļ�ѧ����ʽΪ��2Mg+CO2
2FeCl3����2��SO2���������ԣ����л�ԭ�ԣ��仹ԭ�Խ�ǿ�������Խ���������SO2+2H2S=3S+2H2O����3��þ����������������ȼ�գ�Ҳ�����ڶ�����̼��ȼ�գ���Ӧ�Ļ�ѧ����ʽΪ��2Mg+CO2 2MgO+C����4����NaOH����ʽ��NaHCO3��Һ��Ӧ�����ӷ���ʽΪ��OH-+HCO3-= CO32-+H2O����5���Ȼ�����ǿ�������ԣ�����Cu���������Ȼ�����Һ�̻���·������ӷ���ʽΪ2Fe3++Cu��2Fe2++Cu2+��
2MgO+C����4����NaOH����ʽ��NaHCO3��Һ��Ӧ�����ӷ���ʽΪ��OH-+HCO3-= CO32-+H2O����5���Ȼ�����ǿ�������ԣ�����Cu���������Ȼ�����Һ�̻���·������ӷ���ʽΪ2Fe3++Cu��2Fe2++Cu2+��
�����Ѷȣ�һ��
3��ѡ���� ���н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ��ȷ���ǣ�������
A����ʳ�׳�ȥůˮƿ�е�ˮ����2CH3COOH+CaCO3�TCa2++2CH3COO-+CO2��+H2O
B������ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2��
C��ϡ�����м������ۡ�2Fe+6H+�T2Fe3++3H2��
D��Ca��HCO3��2��Һ�м���������NaOH��Һ��Ca2++2HCO
+2OH-�TCaCO3��+CO+2H2O
�ο��𰸣�A����ʳ�׳�ȥůˮƿ�е�ˮ������Ӧʵ��Ϊ������̼��Ƶķ�Ӧ����Ӧ�����ӷ���ʽΪ��2CH3COOH+CaCO3�TCa2++2CH3COO-+CO2��+H2O����A��ȷ��
B������ˮ��Ӧ�����������ƺ������������ӷ���ʽ��ɲ��غ㣬��ȷ�����ӷ���ʽΪ��2Na+2H2O�T2Na++2OH-+H2������B����
C��ϡ�����м������۷�Ӧ�����������Ӻ���������ȷ�����ӷ���ʽΪ��2Fe+2H+�TFe2++H2������C����
D����������������̼��������Ӳ��ִ��ڣ���ȷ�����ӷ���ʽΪ��Ca2++HCO3-+OH-�TCaCO3��+H2O����D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ�У���ȷ���ǣ�?��
A����Na2O2����Ͷ��H218O�У�2H218O��2Na2O2 = 4OH����4Na����18O2��
B��1mol��L��NaAlO2��Һ��2.5 mol��L��HCl�����������Ȼ�ϣ�2AlO2�� + 5 H��=Al(OH)3����Al3����H2O
C��̼��������Һ����������������Һ��ϣ�HCO3��+Ba2��+OH��=BaCO3��+H2O
D����������Һ�������Һ��ϣ�SiO32��+ 2H�� = H2SiO3��
�ο��𰸣�B
���������A������Na2O2������������ʱ��ԭ����ˮû�в���������ԭ��Ӧ��18OӦ�������������У�B����ȷ��C����������������Ӧ����ȫ��Ӧ��Ba2����OH���Ĺ�ϵӦΪ1:2��D�����������ᣬ���ܲ�
�����Ѷȣ�һ��
5��ѡ���� �����з�Ӧ�У������ӷ���ʽ������H+?+ OH��= H2O��ʾ���ǣ�?��
A��Mg(OH)2��Һ��ϡ����
B��Cu(OH)2��HNO3
C��NaOH��Һ��HNO3��Һ
D��Ba(OH)2��Һ��ϡH2SO4
�ο��𰸣�C
����������������ӷ���ʽ��֪������ǿ���ǿ��֮��ķ�Ӧ���ҷ�Ӧ��û�г������ɣ����Է���������Ӧ����ѡ��C��������þ��������ͭ�����������ѡ��D�л��������ᱵ��������ѡC��
�����Ѷȣ���