微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 离子键的强弱主要决定于离子半径和离子电荷值。一般规律是:离子半径越小,电荷值越大,则离子键越强。试分析:
①K2O?②CaO?③MgO?的离子键由强到弱的顺序是
A.③②①
B.③①②
C.②①③
D.①②③
参考答案:A
本题解析:离子半径是镁离子小于钙离子小于钾离子,因此离子键最强的是氧化镁,其次是氧化钙,所以正确的答案是A。
本题难度:一般
2、选择题 按体积比2∶3混合的N2与CO2 112.8 g在标准状况下体积为
A.22.4 L
B.44.8 L
C.67.2 L
D.89.6 L
参考答案:C
本题解析: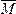 (混)=
(混)=  ="37.6" g・mol-1,故混合气体的物质的量n=
="37.6" g・mol-1,故混合气体的物质的量n=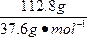 ="3" mol,故体积为3 mol×22.4 L・mol-1="67.2" L。
="3" mol,故体积为3 mol×22.4 L・mol-1="67.2" L。
本题难度:简单
3、选择题 设NA是阿伏加德罗常数的数值,下列说法正确的是
A.1mol Al3+离子含有的核外电子数为10NA
B.1mol Cl2与足量的铁反应,转移的电子数为3NA[来
C.10L pH=1的硫酸溶液中含有的H+离子数为2NA
D.10L pH=13的NaOH溶液中含有的OH-离子数为NA
参考答案:AD
本题解析:1个铝离子含有10个电子,A正确。氯气的还原产物是氯离子,所以1mol氯气在反应中只能得到2mol电子,B不正确。pH=1的硫酸溶液中氢离子浓度为0.1mol/L,所以氢离子的物质的量为10L×0.1mol/L=1mol,C不正确。pH=13的NaOH溶液中氢离子浓度为10-13mol/L,则OH-的浓度为0.1mol/L,所以其物质的量为10L×0.1mol/L=1mol,D正确。答案选AD。
本题难度:一般
4、选择题 常温下,下列气体不能共存的是
A.NO和CO2
B.SO2和O2
C.NH3和HCl
D.NH3和O2
参考答案:C
本题解析:分析:常温下,能相互反应的气体不能共存.
解答:A.常温下,一氧化氮和二氧化碳不反应,所以能共存,故A错误;
B.常温下,二氧化硫和氧气不反应,但在催化剂、加热条件下,二氧化硫和氧气能反应生成三氧化硫,故B错误;
C.氨气和氯化氢气体相遇有白烟生成,白烟是氯化铵固体颗粒,所以氯化氢和氨气不能共存,故C正确;
D.氨气和氧气在常温下不反应,但高温、高压、催化剂条件下能反应生成一氧化氮,所以常温下氨气和氧气在常温下能共存,故D错误;
故选C.
点评:常温下能相互反应的气体不能共存,明确物质的性质是解本题关键,难度不大.
本题难度:困难
5、选择题 下列化合物不能通过单质直接化合而制得的是
A.CuCl2
B.AlCl3
C.FeCl2
D.NaCl
参考答案:C
本题解析:分析:A、根据铜和氯气反应生成氯化铜的性质判断.
B、根据铝和氯气反应生成氯化铝的性质判断.
C、根据铁和氯气生成氯化铁的性质判断.
D、根据钠和氯气生成氯化钠的性质判断.
解答:A、单质铜和氯气化合生成CuCl2,故A不符合;
B、铝和氯气反应生成AlCl3,故B不符合;
C、铁和氯气反应生成FeCl3,故C符合;
D、钠和氯气生成NaCl,故D不符合;
故选:C.
点评:本题主要考查铁、铜、钠、氯气等物质的化学性质,只有熟练掌握化学性质才能解答好本题.
本题难度:困难