|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
<来源:91exam .org!-- | -->
1、选择题 将同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl-完全沉淀,则需同物质的量浓度的
AgNO3溶液的体积比为
[? ]
A.1∶2∶3
B.3∶2∶1
C.1∶1∶1
D.6∶3∶2
参考答案:A
本题解析:
本题难度:简单
2、选择题 在室温下,下列叙述正确的是( )
A.将1?mL?1.0×10-5mol/L盐酸稀释到1000?mL,得到pH=8?的盐酸
B.将1?mL?pH=3的一元酸溶液稀释到10?mL,若溶液的pH<4,则此酸为弱酸
C.用pH=1的盐酸分别中和1?mL?pH=13?NaOH溶液和氨水,NaOH消耗盐酸的体积大
D.pH=2的盐酸与pH=1的硫酸比较,2?c(Cl-)=c(SO42-)
参考答案:A、将1?mL?1.0×10-5mol/L盐酸稀释到1000?mL,得到盐酸pH接近7,不可能大于7,故A错误;
B、一元强酸稀释10倍,pH增大一个单位,一元弱酸稀释10倍,弱酸存在电离平衡,pH增大小于一个单位;将1mLpH=3的一元酸溶液稀释到10 mL,若溶液的pH<4,则此酸为弱酸,故B正确;
C、用pH=1的盐酸分别中和1mLpH=13的NaOH溶液和氨水,氨水存在电离平衡,所以氨水消耗盐酸的体积大,故C错误;
D、pH=2的盐酸与pH=1的硫酸比较,依据HCl=Cl-+H+;H2SO4=2H++SO42-;c(Cl-)=0.01mol/L,而c(SO42-)=0.05mol/L,即5c(Cl-)=c(SO42-),故D错误;
故选B.
本题解析:
本题难度:简单
3、选择题 将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg?/mL,则该盐酸的物质的量浓度是
A.mo1?L-1
B.mol?L-1
C.mol?L-1
D.mol?L-1
参考答案:D
本题解析:分析:利用n= 计算物质的量,利用溶剂和溶质的质量来计算溶液的质量,由溶液的质量和密度可计算溶液的体积,最后利用c= 计算物质的量,利用溶剂和溶质的质量来计算溶液的质量,由溶液的质量和密度可计算溶液的体积,最后利用c= 计算盐酸的物质的量浓度. 计算盐酸的物质的量浓度.
解答:标准状况下的aLHCl(g),
n(HCl)=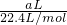 = =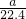 mol, mol,
溶液的质量为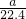 mol×36.5g/mol+1000g, mol×36.5g/mol+1000g,
溶液的体积为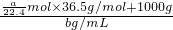 ×10-3L, ×10-3L,
由c= 可知, 可知,
c=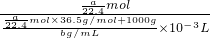 = =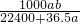 mol/L, mol/L,
故选D.
点评:本题考查物质的量浓度的计算,明确溶液的体积、质量、密度的关系及物质的量浓度的计算公式即可解答,难度不大.
本题难度:简单
4、选择题 某硝酸的物质的量浓度为c?mol・L-1,溶质的质量分数为a%,则此溶液的密度(g・cm-3)为
[? ]
A.63c/a?
B.6.3a/c
C.6.3c/a?
D.63a/c
参考答案:C
本题解析:
本题难度:简单
5、选择题 实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是
[? ]
A.950 mL,111.2 g
B.500 mL,117 g
C.1 000 mL,117 g
D.1 000 mL,111.2 g
参考答案:C
本题解析:
本题难度:简单
|