微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2。下列说法正确的是?
Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2。下列说法正确的是?
A.恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,Ni(CO)4的百分含量将增大
B.在80 ℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol・L-1,则此时v(正)<v(逆)
C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动
D.上述生成Ni(CO)4(g)的反应为吸热反应
参考答案:AB
本题解析:A.恒温恒容下,向容器中再充入少量Ni(CO)4(g),由于压强的影响远大于浓度增大的影响,所以反应容器内的气体压强增大。增大压强,化学平衡会向气体体积减小的方向移动,所以对该反应来说,平衡正向移动,所以达新平衡时,Ni(CO)4的百分含量将增大。正确。B.在80 ℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol・L-1,由于此时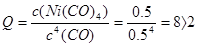 则此时v(正)<v(逆),平衡逆向移动。正确。C.恒温恒压下,向容器中再充入少量的Ar,由于反应混合物的浓度都没有发生变化,所以上述平衡不发生移动。错误。D.因为升高温度,化学平衡常数减小,说明升高温度,平衡逆向移动,因此上述生成Ni(CO)4(g)的反应为放热反应。错误。
则此时v(正)<v(逆),平衡逆向移动。正确。C.恒温恒压下,向容器中再充入少量的Ar,由于反应混合物的浓度都没有发生变化,所以上述平衡不发生移动。错误。D.因为升高温度,化学平衡常数减小,说明升高温度,平衡逆向移动,因此上述生成Ni(CO)4(g)的反应为放热反应。错误。
本题难度:一般
2、简答题 设在某温度时,在容积为1L的密闭容器内,把氮气和氢气两种气体混合,反应后生成氨气.实验测得,当达到平衡时,测得氮气和氢气的浓度各为2mol/L,该温度下的平衡常数为0.5625则
(1)平衡时氨气的浓度为______
(2)求起始加入氮气的浓度
(3)反应前混合气体的平均分子量.
参考答案:达到平衡时,测得氮气和氢气的浓度各为2mol/L,该温度下的平衡常数为0.5625,
(1)根据平衡常数表达式k=c2(NH3)c(N2)?c3(H2)可知,c2(NH3)2×2=0.5625,解得c(NH3)=1.5mol/L,
故答案为:1.5mol/L;
(2)根据N2+3H2?2NH3,可知氮气的浓度变化量为1.5mol/L×12=0.75mol/L,故氮气的起始浓度为2mol/L+0.75mol/L=2.75mol/L,
答:氮气的起始浓度为2.75mol/L.
(3)根据N2+3H2?2NH3,可知氢气的浓度变化量为1.5mol/L×32=2.25mol/L,故氮气的起始浓度为2mol/L+2.25mol/L=4.25mol/L,
故反应前混合气体中氮气与氢气的物质的量之比为2.75mol/L:4.25mol/L=11:17,故反应前混合气体的平均相对分子质量为11×14+17×211+17=6.7,
答:反应前混合气体的平均相对分子质量为6.7.
本题解析:
本题难度:一般
3、选择题 对于反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A.K=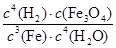
B.K=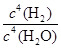
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
参考答案:B
本题解析:化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应式3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)可知,该反应的平衡常数K=
Fe3O4(s)+4H2(g)可知,该反应的平衡常数K=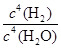 ,A不正确,B正确;C、平衡常数只与温度有关系,所以增大c(H2O)或减小c(H2),该反应的平衡常数不变,C不正确;D、平衡常数只与温度有关系,所以改变反应的温度,平衡常数一定变化,D不正确,答案选B。
,A不正确,B正确;C、平衡常数只与温度有关系,所以增大c(H2O)或减小c(H2),该反应的平衡常数不变,C不正确;D、平衡常数只与温度有关系,所以改变反应的温度,平衡常数一定变化,D不正确,答案选B。
本题难度:一般
4、选择题 碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)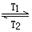 WI2(g)?ΔH<0(温度T1<T2)。下列说法正确的是
WI2(g)?ΔH<0(温度T1<T2)。下列说法正确的是
A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W,W重新沉积到灯丝上
B.灯丝附近温度越高,WI2(g)的转化率越低
C.该反应的平衡常数表达式是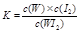
D.利用该反应原理可以提纯钨
参考答案:AD
本题解析:依题意,T1低于T2,高温时WI2(g)分解为W(s)和I2(g),故A项正确;焓变小于0,说明正反应是放热反应,升高温度,有利于WI2(g)分解,温度越高,WI2(g)越容易分解,WI2(g)的转化率越高,故B项错误;固体物质不能写入平衡表达式,因为其浓度是常数,根据平衡常数定义可知,K=c(WI2)/c(I2),故C项错误;根据该反应原理,粗钨置于低温区,在较低温度时与I2(g)发生化合反应,生成的WI2(g)扩散到高温区时,发生分解反应,生成纯净的W(s)留在高温区,而I2(g)扩散到低温区继续与粗钨循环反应,因此可以提纯钨,故D项正确。
本题难度:一般
5、选择题 向2L密闭容器里充入2molM和一定量的N,发生如下反应:M(g)+N(g)?E(g)当反应进行到4min时,测知M的浓度为0.2mol/L;反应进行到2min时,密闭容器中M的物质的量浓度为( )
A.等于0.6mol/L
B.小于0.6mol/L
C.等于0.8mol/L
D.大于0.8mol/L
参考答案:B
本题解析:
本题难度:简单