| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《原电池原理》考点强化练习(2017年押题版)(十)
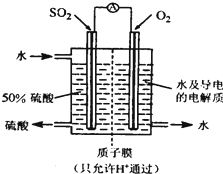 参考答案:A.通入氧气的电极上,氧气得电子发生还原反应,所以通入氧气的电极是正极,故A错误; 本题解析: 本题难度:简单 2、选择题 下列各组的电极材料和电解液,能组成原电池的是 参考答案:A 本题解析:构成原电池的条件是活泼性不同的金属,导线连接后插入到电解质溶液中,据此可知选项A可以组成原电池。B中乙醇是非电解质,C中金属和稀硫酸不反应,不是自发进行的,D中电极是相同的,答案选A。 本题难度:一般 3、填空题 (12分)(1)右图为阳离子交换膜法电解饱和食盐水(滴有酚酞)原理示意图,E口产生H2,电解食盐水的离子方程式为:?,溶液变红色的是:?区(填A或B)。 参考答案:⑴2Cl-+2H2O 本题解析:(1)电解时在溶液中阳离子Na+、H+的放电能力H+ >Na+,所以在阴极发生反应:2H++2e-= H2↑,随着H+的不断放电,破坏了附近的水的电离平衡,最终使附近的水溶液显碱性,所以滴加酚酞溶液变为红色。即B区溶液变为红色;由于阴离子的沸点能力:Cl->OH-,在阳极Cl-放电产生氯气2Cl―2e-= Cl2↑,电解的总方程式为:2Cl-+2H2O 本题难度:一般 4、填空题 (7分)如图所示 参考答案:(7分) (1) Cu (1分) (2) Ag+ + e-=Ag (2分)、 (3)Cu+2Ag+=2Ag+Cu2+ (2分) 本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。铜比银活泼,所以铜是负极,失去电子。银是正极,溶液中银离子得到电子,被还原而析出。 本题难度:一般 5、选择题 下列有关电化学的示意图正确的是( ) 参考答案:D 本题解析:A项,Zn为负极;B项,Zn应放在ZnSO4溶液中,Cu应放在CuSO4溶液中,图示装置不会构成原电池,而是在左烧杯中直接发生化学反应;C项,电解精炼铜,应将粗铜作阳极,精铜作阴极;D项,电解饱和食盐水,在阴极产生H2,阳极产生Cl2,正确。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《与量有关的.. | |