��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����Ԫ�ص�ԭ�����γɲ�ͬ����ʱ�������γ����Ӽ��������γɹ��ۼ����ǣ�������
A��K
B��Ca
C��I
D��Ne
�ο��𰸣�A��K�ǻ��ý��������Լ�Ԫ�����γɲ�ͬ����ʱ��ֻ���γ����Ӽ�����A����
B�����ǻ��ý��������Ը�Ԫ�����γɲ�ͬ����ʱ��ֻ���γ����Ӽ�����B����
C�������γɲ�ͬ����ʱ���ͻ��ý������γ����Ӽ�����NaI���ͷǽ������γɹ��ۼ�����HI�����Ե����γɲ�ͬ����ʱ�������γ����Ӽ��������γɹ��ۼ�����C��ȷ��
D��Ne��ϡ�����壬���ʽ��ȶ���һ�㲻���������ʷ�����ѧ��Ӧ����D����
��ѡC��
���������
�����Ѷȣ�һ��
2��ѡ���� �Ӻ�ˮ����ȡ�������·�Ӧ��5NaBr+NaBrO3+3H2SO4�T3Br2+3Na2SO4+3H2O����÷�Ӧ��������ԭ��Ӧԭ���������Ƶ���
A.2NaBr+Cl2�T2NaCl+Br2
B.C+CO22CO
C.2H2S+SO2�T2H2O+3S��
D.AlCl3+3NaAlO2+6H2O�T4Al��OH��3��+3NaCl
�ο��𰸣�BC
���������������NaBr�е���Ԫ�ػ��ϼ�Ϊ-1�ۣ�NaBrO3����Ԫ�صĻ��ϼ�Ϊ+5�ۣ����������0�۵��嵥�ʣ�����������ԭ��Ӧ�еĹ��з�Ӧ���ͣ�
���A�����ϼ۱仯�ķֱ�����Ԫ�غ���Ԫ�أ����ǹ��з�Ӧ���ͣ���A����
B�����ϼ۱仯����̼Ԫ�أ�һ������0�����ߵ�+2�ۣ�һ������+4�۽���+2�ۣ��ǹ��з�Ӧ���ͣ���B��ȷ��
C����Ԫ�صĻ��ϼ۴�-2������0�ۣ����еĴ�+4�۽���0�ۣ�����������ԭ��Ӧ�еĹ��з�Ӧ���ͣ���C��ȷ��
D����Ӧ��û��Ԫ�ػ��ϼ۵ı仯������������ԭ��Ӧ����D����
��ѡBC��
���������⿼��ѧ�������ͽ�����������������ѧ��������ԭ��Ӧ֪ʶ����ȷԪ�ػ��ϼ��ǽⱾ��ؼ����ѶȲ���
�����Ѷȣ���
3�������� ��֪��101 kPaʱ��CO��ȼ����Ϊ283 kJ��mol-1����ͬ�����£���2 mol CH4��ȫȼ������Һ̬ˮ�����ų�������Ϊ1 mol CO��ȫȼ�շų�������6.30���������ȼ�����Ƕ��٣�
��2������CO��CH4��ɵĻ�����干0.75 mol����ȫȼ�����ɶ�����̼�����18 gҺ̬ˮ���ų�����Ϊ?���٣�?
��3��120 �桢101 kPa�£�a mL��CO��CH4��ɵĻ��������b mL O2����ȫȼ�պָ���ԭ�¶Ⱥ�ѹǿ���������������O2ǡ����ȫ��Ӧ������b mL CO2������������CH4���������Ϊ____________������2λС������
����ȼ�պ����������С��a/4 mL����a��b��ϵ����ѧ��ʾʽ��__________________��
�ο��𰸣���1��891.45 kJ��mol-1��2��516.5 kJ ��3����0.33 ��b��5a/4
�����������1�������ȼ����Ϊ��283 kJ��mol-1��6.30��1/2="891.45" kJ��mol-1��
��2�� CO��CH4��ɵĻ�����干0.75 mol����ȫȼ������18 gҺ̬ˮ�������Ϊ0.5 mol,��ȼ�շų�����Ϊ��0.5 mol��891.45 kJ��mol-1="445.725" kJ���������COΪ0.25 mol����ȼ�շų�����Ϊ��0.25 mol��283 kJ��mol-1="70.75" kJ����0.75 mol���������ȫȼ�չ��ų�516.5 kJ������
��3������������CO��CH4������ֱ�Ϊx��y��������֪��a=b��x+y=b��1/2x+2y=b����֮��y=b/3�����������CH4���������Ϊ��b/3��b=0.33��
��CO��CH4ȼ�յĻ�ѧ����ʽ�ֱ�Ϊ��2CO+O2====2CO2��CH4+2O2====CO2+2H2O����������ʽ���������С����COȼ����ɵģ������Сa/4��CO���ӦΪa/2������ȫȼ����������a/4������a/2����������a��Ϊ��֤���������ȫȼ�չ���b��5a/4��
�����Ѷȣ���
4��ѡ���� ��������������ǣ�������
A�����෴�������֮����������Ϊ���Ӽ�
B������Ԫ����ǽ���Ԫ�ػ���ʱ��һ���γ����Ӽ�
C��ijԪ�ص�ԭ�������ֻ��һ�����ӣ�����±�ؽ��ʱ���γɵĻ�ѧ����һ�������Ӽ�
D��ϡ�������в����ڻ�ѧ��
�ο��𰸣�A�����Ӽ��еľ������ð��������ͳ�������A����
B�����ý�������÷ǽ���֮���γ����Ӽ�����̫���ý���Ԫ����ǽ���Ԫ�ػ���ʱ��һ���γ����Ӽ�����AlCl3�ǹ��ۻ������B��ȷ��
C��ԭ�������ֻ��һ�����ӣ���ԭ�ӿ���ΪHԭ�ӣ���±�ؽ��ʱ���γɵĻ�ѧ���ǹ��ۼ�����C��ȷ��
D��ϡ����������ǵ�ԭ�ӷ��ӣ���D��ȷ��
��ѡ��A
���������
�����Ѷȣ���
5��ѡ���� ����˵�����ʾ��������ȷ����
A�����������������������ֱ���ȫȼ�գ����߷ų���������
B����C��ʯī�� C�����ʯ�� ��H��+19 kJ��mol-1��֪�����ʯ��ʯī�ȶ�
C�����ʯ�� ��H��+19 kJ��mol-1��֪�����ʯ��ʯī�ȶ�
C����101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽΪ��H2��g��+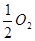 (g)====H2O(l) ��H��+285.8 kJ��mol-1
(g)====H2O(l) ��H��+285.8 kJ��mol-1
D����ϡ��Һ�У�H+��aq��+OH-(aq)====H2O(l) ��H����57.3 kJ��mol-1������0.5 molŨ������Һ�뺬1 mol NaOH����Һ��ϣ��ų�����������57.3 kJ
�ο��𰸣�D
��������������������������������ĸߣ��ʵ��������������������ֱ���ȫȼ�գ�ǰ�߷ų��������࣬A�������C��ʯī�� C�����ʯ�� ��H="+19" kJ��mol-1�����ȵģ���˵��ʯī�������Ƚ��ʯ�ĵͣ�ʯī�Ƚ��ʯ�ȶ���B�����C��Ҳ����ȷ����HӦΪ���ģ�����H="-285.8" kJ��mol-1��D�����Ũ����ϡ�ͷ��ȣ��ʽ�0.5 molŨ������Һ�뺬1 mol NaOH����Һ��ϣ�����1 molˮ�ų�����������57.3 kJ��D����ȷ��
C�����ʯ�� ��H="+19" kJ��mol-1�����ȵģ���˵��ʯī�������Ƚ��ʯ�ĵͣ�ʯī�Ƚ��ʯ�ȶ���B�����C��Ҳ����ȷ����HӦΪ���ģ�����H="-285.8" kJ��mol-1��D�����Ũ����ϡ�ͷ��ȣ��ʽ�0.5 molŨ������Һ�뺬1 mol NaOH����Һ��ϣ�����1 molˮ�ų�����������57.3 kJ��D����ȷ��
�����Ѷȣ���