微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某探究小组用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速度的因素。
实验药品:2.0 mol/L盐酸、4.0 mol/L盐酸、2.0 mol/L硫酸、4.0 mol/L硫酸、相同大小的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0 mL,金属用量均为9.0 g。
Ⅰ.甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
反应进程
(分钟)
| 1
| 2
| 5
| 15
| 20
|
4.0 mol/L
盐酸
| 少量气泡
| 较多气泡
| 大量气泡
| 反应剧烈
| 铝片耗尽
|
2.0 mol/L
硫酸
| 无明显现象
| 极少量
气泡
| 少量气泡
|
4.0 mol/L
硫酸
| 无明显现象
| 少量气泡
| 有比较连续的气泡
|
?
请回答下列问题:
(1)写出铝与盐酸反应的离子方程式:?。
(2)反应在1~15min内,铝与盐酸的反应速率逐渐增大,其原因是?。
(3)根据以上探究“铝与稀盐酸和稀硫酸的反应速率存在差异的原因”,你能对原因作出哪些假设或猜想:?(写出一种即可)。
Ⅱ.乙同学设计了如下影响反应速率因素的实验。请你根据实验目的帮助该同学完成以下实验设计表:
实验目的
| 实验
编号
| 温度
/℃
| 金属铝的
形态
| 盐酸浓度
/mol・L-1
|
1.实验①和②探究盐酸浓度对该反应速率的影响;
2.实验①和③探究温度对该反应速率的影响;
3.实验①和④探究金属规格(铝片、 铝粉)对该反应速率的影响
| ①
| 25
| 铝片
| 4.0
|
②
| ?
| ?
| ?
|
③
| ?
| ?
| ?
|
④
| ?
| ?
| ?
|
?
参考答案:Ⅰ.(1)2Al+6H+=2Al3++3H2↑ (2)反应放出热量,温度升高,使化学反应速率加快 (3)Cl-能够促进金属铝与H+的反应(或SO42-对H+与金属铝的反应起阻碍作用) Ⅱ.如下表所示:
实验编号
温度/℃
金属铝的形态
盐酸浓度/mol・L-1
②
25
铝片
2.0
③
50
铝片
4.0
④
25
铝粉
4.0
?
注:③中温度填其他合理答案也可
本题解析:Ⅰ.(2)1~15 min内铝与盐酸的反应速率逐渐增大的原因主要与反应温度有关,因为该反应是放热反应。(3)比较第1组和第2组(相同H+浓度的盐酸和硫酸),二者的区别在于阴离子不同,从而导致反应速率差别较大,故可得出有关假设:Cl-能够促进金属铝与H+反应或SO42-对H+与金属铝的反应起阻碍作用。Ⅱ.要完成实验设计,必须明确对比实验的目的。因为实验①和②是探究盐酸浓度对该反应速率的影响,故只改变②中盐酸的浓度;实验①和③是探究温度对该反应速率的影响,故只改变③中的反应温度;实验①和④是探究金属规格(铝片、铝粉)对该反应速率的影响,故只改变④中金属铝的形态。
本题难度:一般
2、实验题 (10分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1) 定性分析:如图甲可通过观察____________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________________________________________________________,
写出H2O2在二氧化锰作用下发生反应的化学方程式
____________________________________________________________________。
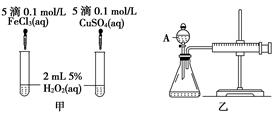
(2) 定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是___________________________________________________________。
检查乙装置气密性的方法是
____________________________________________________________________。
(3) 0.6 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,发生如下反应:
2X(g)+Y(g)===nZ(g)+2W(g), 2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L・min),则前2 min内,用X的物质的量浓度变化表示的平均反应速率为________;2 min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________。
(4) 在一定温度下,反应:2A(s)+2B(g) 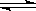 ?C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
?C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
A.容器内的压强不随时间而变化
B.混合气的密度不再随时间而变化
C.A的质量不再改变
D.平衡混合气体的平均相对分子质量不再改变
参考答案:(1)反应产生气泡快慢;控制阴离子相同,排除阴离子的干扰
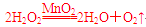
(2)分液漏斗 收集40mL气体所需要的时间 关闭A上的玻璃旋塞,将针筒的活塞拉出(或推进)一段后松开,活塞能回到原来的位置说明气密性良好(其他答案合理也给分)
(3)v(X)=v(W)=0.05 m ol・L-1・min-1; 0.25 mol/L;4
(4)A
本题解析:(1)催化剂的不同会引起反应速率的不同,所以根据反应中产生气泡的快慢来定性分析催化剂的催化效果。为了是实验具有可比性,应该使溶液中的阴离子也相同,这样才能排出阴离子不同可能组成的干扰。
(2)从外观分析A是分液漏斗,收集相同的体积,因此需要测量所用时间的长短。由于装置的右侧是带有活塞的针筒,所以检验其气密性时不能利用传统的方法检验,正确的方法是关闭A上的玻璃旋塞,将针筒的活塞拉出(或推进)一段后松开,活塞能回到原来的位置说明气密性良好,否则漏气。
(3)以Z的物质的量浓度变化表示的反应速率为0.1 mol/(L・min),因此生成Z的物质的量是0.1 mol/(L・min)×2L×2min=0.4mol,同时生成W是0.2mol,因为物质的变化量之比是相应的化学计量数之比,所以n等于4.。因为物质的量的变化量和相应的化学计量数是成正比的,所以速率之比应该是相应的化学计量数之比,故用X的物质的量浓度变化表示的平均反应速率也是0.05 mol/(L・min)。生成0.2molW,就必然消耗0.1molY,则剩余Y是0.5mol,所以2 min末时Y的物质的量浓度为0.25mol/L。
(4)因为反应前后气体的体积是不变的,所以在反应过程中压强始终是不变的,A不正确。密度是混合气的质量和容器容积的比值,容积不变,但混合气的质量是变化的,所以当混合气的密度不再随时间而变化时,可以说明达到平衡状态。A的质量不再改变,说明正逆反应速率相等,因此选项C正确。混合气体的平均相对分子质量是混合气的质量和混合气的物质的量的比值,混合气的物质的量不变,但质量是变化的,因此当平衡混合气体的平均相对分子质量不再改变时可以说明已经达到平衡状态。
本题难度:一般
3、选择题 对于反应:CaCO3+2HCl=CaCl2+ H2O+CO2↑,下列说法正确的是?
?[? ]
A.用HCl和CaCl2表示的反应速率数据不同,但所表示的意义相同
B.不能用CaCO3的浓度变化来表示反应速率,但可用水来表示
C.用H2O和CO2表示的化学反应速率相同
D.用CaCl2浓度的减小表示其反应速率
参考答案:A
本题解析:
本题难度:简单
4、选择题 一定温度下,向容积为2L的密闭容器通入两种气体后发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是(?)
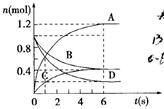
A.该反应的化学方程式为3B+4D=6A+2C
B.反应进行到6s时υ(B)=υ(C)
C.反应进行到6s时,用B表示的平均反应速率为0.05mol・L-1・s-1
D.反应进行到6s时,反应停止了
参考答案:C
本题解析:高考图像可知,B、D的物质的量减小,A、C的物质的量增加,因此B、D是反应物,A、C是生成物。反应进行到6s是,各种物质的浓度不再发生变化,反应达到平衡状态,此时B和D分别减少了0.6mol、0.8mol,A、C的物质的量分别增加了1.2mol、0.4mol。根据物质的量的变化量之比是相应的化学计量数之比可知,该反应的方程式是3B+4D 6A+2C,选项A不正确;反应进行到6s时反应达到平衡状态,则2υ(B)=3υ(C),B不正确;反应进行到6s时,用B表示的平均反应速率为
6A+2C,选项A不正确;反应进行到6s时反应达到平衡状态,则2υ(B)=3υ(C),B不正确;反应进行到6s时,用B表示的平均反应速率为 =0.05mol・L-1・s-1,C正确。平衡时正逆反应速率相等,但不为0,选项D不正确,答案选C。
=0.05mol・L-1・s-1,C正确。平衡时正逆反应速率相等,但不为0,选项D不正确,答案选C。
点评:该题是中等难度的试题,试题贴近高考,基础性强,有利于培养学生的逻辑推理能力和发散思维能力。答题时注意根据图中物质的变化确定反应物和生成物,并能依据变化量之比是相应的化学计量数之比进行计算。
本题难度:一般
5、实验题 催化剂在生产和科技领域起到重大作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

(1)定性分析:如图甲可通过观察?,定性比较得出结论。同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论________(填“合理”或“不合理”),理由是______________________。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是? ?。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①实验时放出气体的总体积是?mL。
②放出1/3气体所需时间为 ??min。
③计算H2O2的初始物质的量浓度_____________。 (请保留两位有效数字)
④A、B、C、D各点反应速率快慢的顺序为_____>____>____>____。
⑤?解释④反应速率变化的原因? ___? _____。
参考答案:(共14分)
(1)产生气泡的快慢(2分),?不合理(2分) ?阴离子种类不同(2分)
(2)产生40mL气体所需的时间(1分)
①60 mL?(1分);?②1 min (1分) ;③ 0.11 mol・L-1(2分);
④D>C>B>A (1分);?⑤随着反应的进行,浓度减小,反应速率减慢 (2分)
本题解析:(1)甲中催化剂不同,则可以通过产生气泡的快慢定性比较得出结论。由于加入的盐中阴离子不同,所以不能通过观察甲中两支试管产生气泡的快慢,得出Fe3+和Cu2+对H2O2分解的催化效果。
(2)要比较外界条件对反应速率的影响,则需要测定产生40mL气体所需的时间来进行定量测定和计算。
(3)①根据图像可知,实验时放出气体的总体积是60ml。
②放出1/3气体大约是20ml,所需时间为1min。
③最终生成氧气的体积是60ml,物质的量是0.06L÷22.4L/mol=0.0027mol
双氧水分解的方程式是
2H2O2=2H2O+O2↑
2mol? 1mol
0.0054? 0.0027
所以双氧水的浓度是0.0054mol÷0.05L=0.11 mol・L-1
④反应速率越快,斜率越大,则A、B、C、D各点反应速率快慢的顺序为D>C>B>A。
⑤由于随着反应的进行,反应物浓度逐渐减小,反应速率减慢。
点评:该题是中等难度的试题,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养。有利于培养学生规范严谨的实验设计能力,有助于提升学生的学科素养。解答时须理清化学反应速率与催化剂间的关系以及速率与图象间的关系。
本题难度:一般