微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 m g铝镁合金与一定浓度的稀硝酸恰好完全反应(假定硝酸的还原产物只有NO)向反应后的混合溶液中滴加a mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n g,则下列有关该实验的说法中正确的有(?)
①沉淀中氢氧根的质量为(n―m)g
②恰好溶解后溶液中的NO3-离子的物质的量为aVmol
③反应过程中转移的电子的物质的量为
④生成NO气体的体积室温下为
⑤与合金反应的硝酸的物质的量为
A.2项
B.3项
C.4项
D.5项
参考答案:B
本题解析:反应中涉及的电子转移及生成沉淀的反应为:
Mg-2e-=Mg2+? Mg2++2OH-=Mg(OH)2
Al-3e-=Al3+? Al3++3OH-=Al(OH)3
从上式可看出,反应中电子转移数目与沉淀过程中OH-的个数相等;
合金最终生成沉淀,两者质量的差值应该为沉淀中氢氧根的质量,即(n―m)g,物质的量为 ,也就是说反应过程中转移的电子的物质的量也是
,也就是说反应过程中转移的电子的物质的量也是 ;
;
由3e―→NO↑,可得NO的物质的量为 mol,标准状况下的体积为
mol,标准状况下的体积为 ,而室温下无法确定
,而室温下无法确定
离子全部沉淀达到最大值时,溶液为NaNO3溶液,由钠的守恒可知,NaNO3的物质的量与NaOH的物质的量相同,即 mol;也就是合金恰好溶解后溶液中的NO3-离子的物质的量
mol;也就是合金恰好溶解后溶液中的NO3-离子的物质的量 mol;
mol;
由氮的守恒可知,原硝酸溶液中硝酸的物质的量为
故题目中的①③⑤说法正确,故答案为B
本题难度:一般
2、选择题 下列各金属的混合物2.5 g和足量的盐酸反应,放出的H2在标准状况下体积为2.24 L,其中可能的是(? )
A.Zn和Fe
B.Mg和Zn
C.Al和Mg
D.Cu和Fe
参考答案:B
本题解析:假设2.5 g分别是Zn、Fe、Mg、Al,看生成H2比2.24 L多还是少,再据同质量金属与酸反应产生H2量顺序Al>Mg>Fe>Zn判断。
本题难度:简单
3、填空题 已知A~G有如图所示的转化关系(部分生成物已略去),其中A、G为单质,D是能使湿润的红色石蕊试纸变蓝色的气体,E、F均能与NaOH溶液反应。
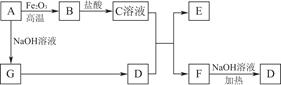
请回答下列问题:
(1)写出F的电子式:____________。
(2)①C溶液与D反应的离子方程式为________________________________________________________________________________________________________________________________________________;
②F溶液与NaOH溶液共热反应的化学方程式为________________________________________________________________________________________________________________________________________________。
(3)①请用离子方程式解释C溶液为何显酸性:________________________________________________________________________________________________________________________________________________,
②F溶液中离子浓度由大到小的顺序为________________________________________________________________________。
(4)将5.4 g A投入200 mL 2.0 mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是________(填代号)。
A.HNO3溶液?B.H2SO4溶液? C.NaOH溶液 ?D.HCl溶液
(5)将1 mol N2和3 mol G及催化剂充入容积为2 L的某密闭容器中进行反应,已知该反应为放热反应。平衡时,测得D的物质的量浓度为a? mol/L。
①如果反应速率v(G)=1.2 mol/(L・min),则v(D)=________mol/(L・min)。
②在其他条件不变的情况下,若起始时充入0.5 mol N2和1.5 mol G达到平衡后,D的物质的量浓度________(填“大于”“小于”或“等于”)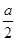 mol/L。
mol/L。
③该条件下的平衡常数为__________________(用含a的代数式表示)。
参考答案:(1)[H∶N?,?H,H ∶H]+[∶Cl?,?∶]-
(2)①Al3++3NH3・H2O=Al(OH)3↓+3NH4+
②NH4Cl+NaOH NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
(3)①Al3++3H2O?Al(OH)3+3H+
②c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(4)D
(5)①0.8 ②小于
③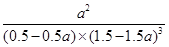 或
或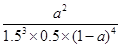
本题解析:由A为单质且能与NaOH溶液和Fe2O3反应可知A为Al,则B为Al2O3,C为AlCl3;由D是能使湿润的红色石蕊试纸变蓝色的气体可知D为NH3,则G为H2,E为Al(OH)3,F为NH4Cl。(1)NH4Cl为离子化合物,NH4+离子中含有四个N-H共价键,故其电子式为[H∶N?,?H,H ∶H]+[∶Cl?,?∶]-。(2)NH3・H2O是弱电解质,不能拆开写,与Al3+反应产物为Al(OH)3。(3)①AlCl3为强酸弱碱盐,水解显酸性;②NH4Cl为强酸弱碱盐,水解显酸性,且其水解反应以及水的电离反应都是程度很微弱的反应,故溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-)。(4)Al与HNO3溶液反应产物为NO或NO2,不是单质,A项错误;0.2 mol Al与0.4 mol的H2SO4溶液或NaOH溶液反应时Al可以反应完全,B、C项错误;D项正确。(5)该反应为N2(g)+3H2(g) 2NH3(g)。①v(NH3)=
2NH3(g)。①v(NH3)=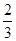 v(H2)=0.8 mol/(L・min);②与原平衡相比,起始时充入0.5 mol N2和1.5 mol G相当于减小压强,平衡向逆反应方向移动,故D的物质的量浓度小于
v(H2)=0.8 mol/(L・min);②与原平衡相比,起始时充入0.5 mol N2和1.5 mol G相当于减小压强,平衡向逆反应方向移动,故D的物质的量浓度小于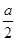 ?mol/L;③由题目所给数据可得该反应的三段式:
?mol/L;③由题目所给数据可得该反应的三段式:
N2(g) + 3H2(g) 2NH3(g)
2NH3(g)
起始浓度?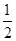 ?mol/L?
?mol/L?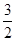 ?mol/L? 0
?mol/L? 0
浓度变化?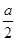 ?mol/L?
?mol/L?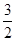 a mol/L? a mol/L
a mol/L? a mol/L
平衡浓度?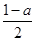 ?mol/L?
?mol/L?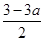 ?mol/L? a mol/L
?mol/L? a mol/L
则K=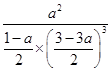 。
。
本题难度:一般
4、填空题 (12分)
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
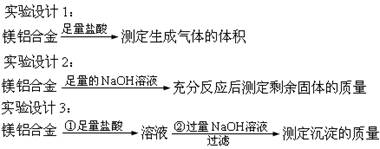
回答下列问题:
(1)上述方案中,能测出Mg的质量分数的方案是?(填写代号,下同)
A.实验设计1? B.实验设计2? C.实验设计3? D.都可以
(2)上述方案中的化学反应体现了Mg、Al的性质是??
A.氧化性? B.还原性? C.酸性? D.碱性
(3)某同学设计了右图装置。该装置适合的实验设计是?
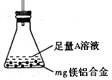

用该装置测定镁铝合金中镁的质量分数,所需的实验操作是
?。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.称量反应前后,装置和药品的总质量
(4)若按实验设计3进行实验。将m g镁铝合金,溶于过量盐酸中,再加入过量的NaOH溶液,可得到白色沉淀,该沉淀物质是?(填化学式);将此沉淀洗净、干燥后,称得质量为w g。求合金中镁的质量分数?;
参考答案:(1)D(2分) (2)B (2分)?(3) B (2分)? B (2分)
(4)Mg(OH)2 (2分)? 12w/29m(2分)
本题解析:(1)设计(1)根据镁铝合金质量及氢气的体积可计算出结果,设计(2)铝能溶于强碱而镁不溶可知剩余的是镁,设计(3)利用Al(OH)3能溶于强碱而Mg(OH)2不溶于强碱可求解;(2)金属和酸反应或和碱反应都表现了还原性;(3)设计1需要气体收集装置,设计3第一步反应完还需要继续加NaOH溶液,所以,此装置只适用于设计2,因镁不溶于NaOH溶液,所以剩余固体即为镁;(4)因Mg(OH)2不溶于NaOH溶液Al (OH)3能溶于NaOH溶液,可知剩余的是Mg(OH)2,根据镁的物质的量等于氢氧化镁的物质的量,质量等于物质的量乘以摩尔质量这一计算式可求出镁的质量,再用镁的质量除以m克乘以100%,即可求出镁的质量分数。
本题难度:简单
5、选择题 将等体积的AlCl3溶液和NaOH溶液混合后,沉淀物中铝元素的物质的量与溶液中铝元素的物质的量相等,则原AlCl3溶液与NaOH溶液的物质的量浓度之比可能是(? )
A.1:3
B.2:5
C.1:5
D.2:7
参考答案:D
本题解析:由于氢氧化铝是两性氢氧化物,能溶于氢氧化钠溶液中,所以溶液中的铝元素,可以是铝离子,也可以是AlO2-,因此根据反应的方程式Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O可知,如果氯化铝过量,则原AlCl3溶液与NaOH溶液的物质的量浓度之比2:3;如果氢氧化钠过量,生成偏铝酸钠,则原AlCl3溶液与NaOH溶液的物质的量浓度之比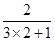 =2:7,答案选D。
=2:7,答案选D。
点评:由于氢氧化铝是两性氢氧化物,能溶于氢氧化钠溶液中,所以在计算生成的氢氧化铝时,应该注意如果氢氧化钠过量时生成的氢氧化铝会溶剂在过量的氢氧化钠中,因此本题应该有2种情况。
本题难度:一般