微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号
| A溶液
| B溶液
|
①
| 20 mL 0.1 mol・L-1H2C2O4溶液
| 30 mL 0.01 mol・L-1KMnO4溶液
|
②
| 20 mL 0.2 mol・L-1
H2C2O4溶液
| 30 mL 0.01 mol・L-1KMnO4溶液
|

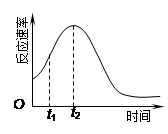
(1) 该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 - (填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),
则在2 min末,c(MnO4-)= mol/L。
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。
(4)小组同学发现反应速率总是如右图,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、② 。
参考答案:(1)浓度 ②>①
(2)0.0052
(3)KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间
(4)产物Mn2+(或MnSO4)是反应的催化剂
本题解析:(1)从题中可以看出H2C2O4溶液的浓度不同,KMnO4溶液而的浓度相同,说明该实验探究的是浓度对对化学反应速率的影响,并且浓度越大,反应速率越快,相同时间内针筒中所得CO2的体积为②>①;(2)中,在2 min末收集了4.48 mL CO2(标准状况下),即得到了0.0002mol CO2,根据2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知,消耗了0.00004mol MnO4-,则剩下的
(30*0.010/1000)-0.00004=0.00026mol,所以c=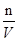 =
= mol/L=0.0052 mol/L;(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(4)刚开始反应的时候,速率并不快,但是后来逐渐加快,这可能是由于反应放热,或者是生成了具有催化作用的物质,例如Mn2+(或MnSO4)。
mol/L=0.0052 mol/L;(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(4)刚开始反应的时候,速率并不快,但是后来逐渐加快,这可能是由于反应放热,或者是生成了具有催化作用的物质,例如Mn2+(或MnSO4)。
考点:影响化学反应速率的原因
点评:该题考查了影响化学反应速率的原因,是一道综合题,这有利于提高学生的综合分析能力,但是该题的难度不大,只有最后一个空有点难度,考生在解答这个空时,要联想到催化剂的作用就可以迎刃而解。
本题难度:困难
2、选择题 对于反应2SO2(g)+O2(g)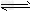 2SO3(g),能增大正反应速率的措施是
2SO3(g),能增大正反应速率的措施是
[? ]
A.通入大量的O2?
B.增大容器容积
C.移去部分SO3?
D.降低体系温度
参考答案:A
本题解析:
本题难度:一般
3、选择题 用铁片与0.1mol/L硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是
A.改用98%浓硫酸
B.加热
C.改用2mol/L硫酸
D.把铁片换成铁粉
参考答案:A
本题解析:A、因浓硫酸具有强氧化性,铁与浓硫酸在加热的条件下反应生成二氧化硫而不生成氢气,故A不能;B、因加热时反应体系的温度升高,所以化学反应速率加快,故B能;C、改用2mol/L的稀硫酸,增大氢离子的浓度,从而加快了生成氢气的反应速率,故C能;D、改用铁粉,增大了铁与硫酸反应的接触面积,因此反应速率加快,故D能,答案选A。
本题难度:一般
4、选择题 决定化学反应速率的主要因素是(?)
① 温度 ② 压强 ③ 催化剂 ④ 浓度 ⑤ 反应物本身的性质
A?①②③④⑤? B?⑤? C?①④? D?①②③④
参考答案:B
本题解析:反应物本身的性质是决定化学反应速率的主要因素,其他因素都是外界条件,所以答案是B。
本题难度:简单
5、选择题 下列体系加压后,对化学反应速率没有影响的是
A.2SO2+O2 2SO3
2SO3
B.CO+H2O(g)  CO2+H2
CO2+H2
C.CO2+H2O H2CO3
H2CO3
D.H++OH- H2O
H2O