微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(氢硫酸)、C(溴化亚铁溶液)、D(碘化钾淀粉溶液)、E(混有SO2的氯化钡溶液)、F(水)、H(紫色石蕊试液)。
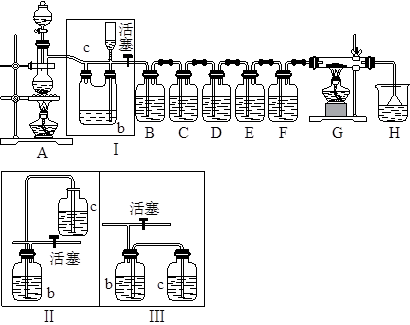
(1)A是氯气发生装置,其离子反应方程式是:__________。
(2)Ⅰ中b瓶内加入的液体最好是____________。
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?________,简要说明理由_____________________________。
(4)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯,回答下列问题:
①怎样证明氯气已充满整个装置?_____________。
②下列装置中的现象是C______________________;
D________;E____________;F________________。
(5)G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出G中反应的化学方程式_______________________。装置F的作用是______________________。
(6)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是______________________________。
参考答案:(1)MnO2+4H++2Cl-(浓)△Mn2++Cl2↑+2H2O
(2)饱和食盐水
(3)Ⅱ可行,Ⅲ不可行 Ⅱ原理同Ⅰ,而Ⅲ中因c瓶口密封,体积不能改变,压强增大会有危险
(4)①观察,当整个装置内充满黄绿色气体时,说明氯气已充满整个装置
②溶液由浅绿色变为深红棕色 溶液变蓝 生成白色沉淀 溶液变为浅黄绿色
(5)C+2H2O+2Cl2△CO2+4HCl 向G中提供反应所需的水蒸气
(6)生成HCl使紫色石蕊试液变红色,剩余的氯气又与水反应生成HClO,起漂白作用,使红色褪去
本题解析:(2)b瓶的作用是贮存多余的Cl2,试剂最好为饱和食盐水。
(3)Ⅱ原理同Ⅰ,可代替Ⅰ;Ⅲ中c瓶口密封,不安全。
(4)①当黄绿色气体充满整个装置时,说明Cl2充满。
②Cl2有强氧化性,可将Fe2+、Br-、I-、SO2氧化为Fe3+、Br2、I2、SO,故C中溶液由浅绿色变为深红棕色;D中溶液变蓝;E中产生白色沉淀BaSO4;F中由于吸收了Cl2变为浅黄绿色。
(5)C+2H2O+2Cl2△CO2+4HCl,F的作用是提供水蒸气。
(6)生成HCl使溶液变红,剩余Cl2与水反应生成HClO又起漂白作用。
本题难度:简单
2、选择题 下列有关新制氯水的叙述,正确的是( )
A.氯水放置数天后,其酸性逐渐增强
B.新制氯水可使紫色石蕊试液先变红后褪色,说明Cl2具有漂白性
C.氯水光照时有气泡逸出,该气体的主要成分是氯气
D.加入一定量CaCO3,盐酸、次氯酸的浓度都将减小
参考答案:A、氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸,酸性比碳酸还弱,但次氯酸不稳定见光易分解,次氯酸分解生成盐酸和氧气,导致溶液中盐酸浓度增大,酸性增强,故A正确.
B、氯气和水反应生成盐酸和次氯酸,溶液呈酸性,向新制氯水中加紫色石蕊试液,溶液呈红色;但次氯酸有漂白性,能使有色物质褪色,所以红色逐渐褪去,起漂白性的物质是次氯酸不是氯气,故B错误.
C、次氯酸不稳定,见光易分解生成盐酸和氧气,所以氯水光照时有气泡逸出,该气体的主要成分是氧气,故C错误.
D、氯气和水的反应方程式为:Cl2+H2O?HCl+HClO,该反应是可逆反应,盐酸和碳酸钙反应导致盐酸浓度变小,平衡向正反应方向移动,次氯酸和碳酸钙不反应,所以导致次氯酸浓度增大,故D错误.
故选A.
本题解析:
本题难度:一般
3、选择题 25℃时,下列关于饱和氯水的叙述中错误的是( )
A.在饱和氯水中加入CaCO3,溶液的pH变大
B.在饱和氯水中通入SO2气体,溶液的pH变小
C.在饱和氯水中通入H2S气体,溶液的pH变小
D.在饱和氯水中加入NaOH使pH=7,所得溶液中离子浓度的关系如下:c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
参考答案:A.在饱和氯水中加入CaCO3,与H+反应,则溶液酸性减弱,pH变大,故A正确;
B.在饱和氯水中通入SO2气体,与Cl2反应生成硫酸和盐酸,酸性增强,pH变小,故B正确;
C.在饱和氯水中通入H2S气体,与Cl2反应生成S和盐酸,酸性增强,pH变小,故C正确;
D.在饱和氯水中加入NaOH使pH=7,c(H+)=c(0H-),由电荷守恒可知,c(Na+)=c(ClO-)+c(Cl-),反应后溶质为NaCl、NaClO、HClO,由Cl2+H2O?HClO+HCl可知,c(Cl-)=c(ClO-)+c(HClO),则离子浓度大小为c(Na+)>c(Cl-)>c(ClO-)>c(HClO),故D错误;
故选D.
本题解析:
本题难度:一般
4、选择题 下列中的实验一定不会出现沉淀现象的是
A.CO2气体通入Na2SiO3溶液中
B.SO2气体通入BaCl2溶液中
C.CO2气体通入饱和Na2CO3溶液中
D.SO2气体通入Ba(OH)2溶液中
参考答案:B
本题解析:A、碳酸的酸性强于硅酸,因此CO2气体通入Na2SiO3溶液中产生硅酸沉淀;B、SO2与氯化钡不反应;C、碳酸氢钠的溶解度小于碳酸钠的溶解度,因此CO2气体通入饱和Na2CO3溶液中产生碳酸氢钠沉淀;D、SO2气体通入Ba(OH)2溶液中可以产生亚硫酸钡沉淀,故答案选B。
本题难度:一般
5、选择题 下列物质中含有自由移动的Cl-的是(?)
A.液氯
B.KClO3
C.NaCl晶体
D.氯水
参考答案:D
本题解析:关键明确氯气本身并无漂白作用,所以它不能使干燥的物质褪色,而是与水反应生成的次氯酸具有漂白作用。
本题难度:一般