微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 用31.6gKMnO4恰好氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸.反应方程式如下:
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(1)标出以上反应电子转移的方向和数目.
(2)有多少摩尔HCl被氧化?______
(3)产生的Cl2在标准状况下的体积为多少?______
(4)求消耗该盐酸溶液的体积?______.
参考答案:(1)反应中高锰酸钾为氧化剂,HCl为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,反应中氧化剂和还原剂得失电子数目相等,反应电子转移的方向和数目为: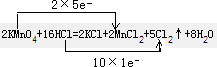 ,
,
答:反应电子转移的方向和数目为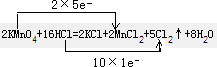 ;
;
(2)31.6gKMnO4的物质的量为31.6g158g/mol=0.2mol,则:
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2165
0.2mol n(HCl) n(Cl2)
所以,n(Cl2)=0.2mol×52=0.5mol,被氧化的HCl生成氯气,故被氧化的HCl的物质的量为0.5mol×2=1mol,故答案为:1mol;
(3)V(Cl2)=0.5mol×22.4L/mol=11.2L,故答案为:11.2L;
(4)消耗的n(HCl)=0.2mol×162=1.6mol,
该盐酸的物质的量浓度为1000×1.19×36.5%36.5mol/L=11.9mol/L,
故消耗盐酸的体积为1.6mol11.9mol/L=0.134L,
故答案为:0.134L.
本题解析:
本题难度:一般
2、选择题 下列化学式既能表示物质的组成,又能表示物质的分子式的是
A.NH4NO3
B.SiO2
C.SO3
D.P
参考答案:C
本题解析:
正确答案:C
A、NH4NO3是离子化合物,没有分子式;B、SiO2是原子晶体,由原子构成;C、SO3是共价化合物由分子构成。D、白磷分子式是P4、红磷分子是Px。
本题难度:一般
3、选择题 下列叙述中,不正确的是(?)
A.原电池负极上发生的反应是氧化反应
B.失电子能力弱的物质获得电子的能力一定强
C.阳离子在氧化还原反应中,可能表现氧化性,也可能表现还原性
D.氯气分子在反应中,作氧化剂的同时也可能是还原剂
参考答案:B
本题解析:B不正确,例如稀有气体原子,既难失去电子,也难得到电子。其余都是正确的,答案选B。
本题难度:简单
4、选择题 .进入人体的O2有2%转化为氧化性极强的“活性氧”,它能加速人的衰老,被称为“生命杀手”,服用含硒(Se)元素的化合物亚硒酸钠(Na2SeO3)能消除人体内的活性氧。有关此过程中Na2SeO3的说法正确的是(?)?
A.作还原剂
B.亚硒酸钠中硒的化合价为+6价
C.既作还原剂又作氧化剂
D.作氧化剂
参考答案:A
本题解析:略
本题难度:一般
5、选择题 “S、T、P”是指?
A.20℃,1大气压
B.273K,101.3KPa
C.293K,1大气压
D.0℃,101.3Pa
参考答案:B
本题解析:略
本题难度:简单