微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是
[? ]
A.NaCl溶液?
B.HCl溶液?
C.NaOH溶液?
D.AgNO3溶液
参考答案:C
本题解析:
本题难度:一般
2、填空题 ( 9分)对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含乙酸钠和对氯酚( )的废水可以通过构成微生物电池除去,其原理如下图所示。
)的废水可以通过构成微生物电池除去,其原理如下图所示。
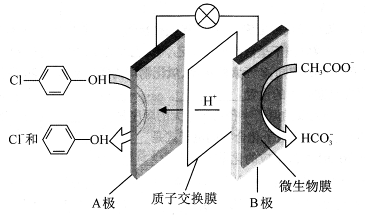
①B是电池的 极(填“正”或“负”);②A极的电极反应式为 。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA ”表示乳酸分子,A-表示乳酸根离子)。
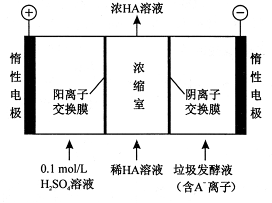
①阳极的电极反应式为 ;
②简述浓缩室中得到浓乳酸的原理 ;
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8 ,此时进人浓缩室的OH-可忽略不计。400 mL10g/L 乳酸溶液通电一段时间后,浓度上升为 145g/L(溶液体积变化忽略不计),则阴极上产生的H2在标准状况下的体积约为 L(乳酸的摩尔质量为90g/ mol )。
参考答案:(1)①负;② +H++2e-=
+H++2e-=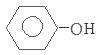 +Cl-;
+Cl-;
(2)①4OH--4e-=2H2O+O2↑;②阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,乳酸浓度增大;③6.72
本题解析:(1)①由于H+向A极板移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,所以B是电池的负极;②A极的电极反应式为 +H++2e-=
+H++2e-= +Cl-;(2) ①在阳极溶液中的阴离子放电,由于OH-的放电能力大于含氧酸根离子,所以在阳极OH-放电,该电极的电极反应式为4OH--4e-=2H2O+O2↑;在阳极发生反应:2H++2e-=H2↑;②浓缩室中得到浓乳酸的原理是在阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,所以乳酸浓度增大;③反应过程中产生的乳酸的质量是0.400 L(145g/L -10g/L)=54g.则乳酸的物质的量是54g÷90g/ mol=0.6mol;因为在反应过程乳酸根离子结合的H+离子的个数与反应过程中放电的H+或OH-的个数相等,所以n(H2)=1/2n(乳酸)=0.3mol,其在标准状况下体积是0.3mol×22.4L/mol=6.72L。
+Cl-;(2) ①在阳极溶液中的阴离子放电,由于OH-的放电能力大于含氧酸根离子,所以在阳极OH-放电,该电极的电极反应式为4OH--4e-=2H2O+O2↑;在阳极发生反应:2H++2e-=H2↑;②浓缩室中得到浓乳酸的原理是在阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,所以乳酸浓度增大;③反应过程中产生的乳酸的质量是0.400 L(145g/L -10g/L)=54g.则乳酸的物质的量是54g÷90g/ mol=0.6mol;因为在反应过程乳酸根离子结合的H+离子的个数与反应过程中放电的H+或OH-的个数相等,所以n(H2)=1/2n(乳酸)=0.3mol,其在标准状况下体积是0.3mol×22.4L/mol=6.72L。
考点:考查电池电极的判断、电解原理的在废水处理中的应用和计算的知识。
本题难度:困难
3、选择题 用石墨做电极电解下列溶液,通电一段时间后溶液的pH变大的是
[? ]
A.NaCl溶液
B.NaOH溶液
C.H2SO4溶液
D.CuSO4溶液
参考答案:AB
本题解析:
本题难度:一般
4、填空题 铝及其化合物在生产生活中具有重要的作用。
(1)铝在元素周期表中的位置是 。
(2)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
①铝的电负性χ的范围是 。
②电负性的数值与元素金属性的关系是 。
③下列实验能比较镁和铝的金属性强弱的是 。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/LAlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al(s)+3O2(g)=2Al2O3(s) ΔH1=-3352 kJ/mol
Mn(s)+O2(g)=MnO2(s) ΔH2= -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是 。
(4)冶炼金属铝时,用石墨做电极电解熔融Al2O3。液态铝在(填“阴”或“阳”) 极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是 。
参考答案:(14分,每空2分)
(1)第3周期第ⅢA族
(2)①电负性数值越大,元素的金属性越弱
② 1.2<χ<1.8
③ c
(3)4Al(s)+ 3MnO2(s)=3Mn(s)+2Al2O3(s) ΔH=
本题解析:
本题难度:困难
5、选择题 臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多。其中高压放电法和电解纯水法原理如下图所示,下列有关说明不正确的是

[? ]
A.高压放电法,反应的原理为:3O2 2O3
2O3
B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物
C.电解法,电极b周围发生的电极反应有:3H2O-6e-=O3+6H+,2H2O-4e-=O2+4H+
D.电解时,H+由电极a经聚合固体电解质膜流向电极b
参考答案:D
本题解析:
本题难度:一般