��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
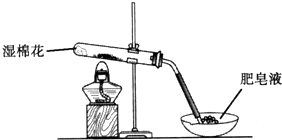
1������� ijͬѧ������ͼ��ʾװ�ý���Fe����ˮ�����ķ�Ӧ��
��1��д��Fe����ˮ������Ӧ�Ļ�ѧ����ʽ______��
��2����ͬѧ��Ӧ��Ĺ����м��������ϡHCl��������Һ��װ����֧�Թ��У�
�����һ֧�Թ��еμ�KSCN��Һ����Һ�ʺ�ɫ������Һ�д��ڵ���������______��
����ڶ�֧�Թ��м����������ۣ��ù����з������Ϸ�Ӧ�����ӷ���ʽ��______��
����������Һ�еμ�NaOH��Һ������һ��ʱ�䣬�ò���Ӧ�е�ʵ��������______��������������ԭ��Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣���1���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�3Fe+4H2O��g�� ����.Fe3O4+4H2��
�ʴ��ǣ�3Fe+4H2O��g�� ����.Fe3O4+4H2��
��2���ٵμ�KSCN��Һ����Һ�ʺ�ɫ��֤����Fe3+����Ӧ��Ĺ�����һ������ʣ������������ᷴӦ�����Ȼ���������Һ�к��������ӣ�
�ʴ��ǣ�Fe3+��Fe2+��H+��
�ڼ����������ۣ�����Fe3+��Ӧ����Ӧ�����ӷ���ʽ�ǣ�2Fe3++Fe�T3 Fe2+����������������Һ�������ǣ�������ɫ������Ѹ��ɻ���ɫ�������ٱ�ɺ��ɫ����Ӧ�Ļ�ѧ����ʽΪ��4Fe��OH��2+O2+2 H2O�T4 Fe��OH��3 ��
�ʴ��ǣ�2Fe3++Fe�T3 Fe2+�� ������ɫ������Ѹ��ɻ���ɫ�������ٱ�ɺ�֣� 4Fe��OH��2+O2+2 H2O�T4 Fe��OH��3 ��
���������
�����Ѷȣ���
2������� ��14�֣�����һ�ֹ���Ԫ�أ�����������õĽ�������ش����и��⣺
��1�������к���һ����̼������(Fe3C)���������Ŀ����и������գ������д��ԵĹ������ʹ����ʯ��ˮ����ǵ����壬�÷�Ӧ�Ļ�ѧ����ʽΪ?��������Ӧ���ɵĴ��Թ��������ڹ������ᣬ�÷�Ӧ�����ӷ���ʽΪ?��
��2����Fe2+��Fe3+�Ĵ������£���ʵ��2SO2+O2+2H2O=2H2SO4��ת������֪����SO2�ķ���ͨ��Fe2+��Fe3+����Һʱ������һ����Ӧ�����ӷ���ʽΪ4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O������һ��Ӧ�����ӷ���ʽΪ?��
��3�����᳧�����ջ�����FeS2������ȡ���ᣬʵ�����������᳧��������Ҫ�ɷ���Fe2O3������FeS��SiO2�����̷��������������̷��Ĺ������£�
 ?
?
����������ϡH2SO4�����У��е��������ɣ�д���÷�Ӧ�����ӷ���ʽ��ֻд����S�ķ�Ӧʽ��������Ӧ����д����?��
������ҺX�м���������м��Ŀ����?��
�ۿ��������ữ�� KMnO4��Һͨ���ζ����ⶨ�̷���Ʒ��FeSO4�������ζ�ʱ������Ӧ�����ӷ���ʽΪ?��
��4����֪Fe(OH)3���ܶȻ�����Ksp��1.1��10-36������ʱ��FeCl3��Һ�еμ�NaOH��Һ������ҺpH=3ʱ��ͨ������˵��Fe3+�Ƿ������ȫ?��
����ʾ����ij����Ũ��С��1.0��10-5 mol?L-1ʱ������Ϊ�����ӳ�����ȫ�ˣ�
�ο��𰸣���1��Fe3C + 3O2 Fe3O4 + CO2��2�֣�? Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O��2�֣�
Fe3O4 + CO2��2�֣�? Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O��2�֣�
��2��2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42- + 4H+��2�֣�
��3����2Fe3+ + H2S = 2Fe2+ + S�� + 2H+��2�֣�
��ʹFe3+��ȫת��ΪFe2+�����Ʊ��������̷����壨2�֣�
��5Fe2+ + MnO4- + 8H+ = 5Fe3++Mn2+ + 4H2O��2�֣�
��4�������c(Fe3��)��1.1��10-3mol?L-1��1��10-5 mol?L-1����Fe3+û�г�����ȫ��2�֣�
�����������1�����ݷ�Ӧ����������֪����Ӧ�ķ���ʽΪFe3C + 3O2 Fe3O4 + CO2��������������������Ԫ�صĻ��ϼۼ��У�2�۵ģ����У�3�۵ģ����Է���ʽΪFe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O��
Fe3O4 + CO2��������������������Ԫ�صĻ��ϼۼ��У�2�۵ģ����У�3�۵ģ����Է���ʽΪFe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O��
��2���������⣬�ܷ�Ӧʽ��ȥ4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O���õ���һ������2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42- + 4H+��
��3�����ڷ�Ӧ�������������ᷴӦ�������⣬�������������ᷴӦ�����������������������������������ʣ�����ʽΪ2Fe3+ + H2S = 2Fe2+ + S�� + 2H+��
����Һ�к��������ӣ����Ա����仹ԭ���������ӣ������۵�������ʹFe3+��ȫת��ΪFe2+�����Ʊ��������̷����塣
�۸��������Һ���������ԣ��ܰ�����������������������������ʽΪ5Fe2+ + MnO4- + 8H+ = 5Fe3++Mn2+ + 4H2O��
��4��pH=3��������Һ��OH����Ũ����10��11mol/L�����Ը����ܶȻ������ı���ʽ
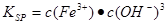 ��֪����Һ��������Ũ����
��֪����Һ��������Ũ����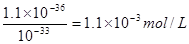 ��1��10-5 mol?L-1����Fe3+û�г�����ȫ��
��1��10-5 mol?L-1����Fe3+û�г�����ȫ��
�����Ѷȣ�һ��
3��ѡ���� ������һ����̼��ԭ14.5 g����������Ļ��������ɵ�����ͨ�������ij���ʯ��ˮ�У����ɳ���25 g����û�������ϲ�������
��Fe2O3��Fe3O4��FeO����FeO��Fe3O4����Fe3O4��Fe2O3����FeO��Fe2O3
A���٢�
B���ڢ�
C���ۢ�
D���٢�
�ο��𰸣�B
���������CO��ԭ��������������CO2��CO2���������Ʒ�Ӧ����̼��ƣ���25g��̼��Ƶ����������ʵ�����25g��100g/mol��0.25mol�������ԭ���غ��֪CO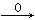 CO2��CaCO3����������������Ԫ�ص����ʵ�����0.25mol����������0.25mol��16g/mol��4g�����������������Ԫ�ص�������14.5g��4g��10.5g�����ʵ�����105.g��56g/mol��0.1875mol�����Խ�����������������Ԫ�صĸ���֮�ȣ�0.1875:0.25��3:4�����������������������������ʵ���֮��1:1��ϼ���������������Ԫ�صĸ���֮�ȣ�3:4,����ѡ��١��ܾ��п��ܣ���ѡ��ڢ۲���������������Ԫ�صĸ���֮�ȣ�3:4,�����ȷ�Ĵ�ѡB��
CO2��CaCO3����������������Ԫ�ص����ʵ�����0.25mol����������0.25mol��16g/mol��4g�����������������Ԫ�ص�������14.5g��4g��10.5g�����ʵ�����105.g��56g/mol��0.1875mol�����Խ�����������������Ԫ�صĸ���֮�ȣ�0.1875:0.25��3:4�����������������������������ʵ���֮��1:1��ϼ���������������Ԫ�صĸ���֮�ȣ�3:4,����ѡ��١��ܾ��п��ܣ���ѡ��ڢ۲���������������Ԫ�صĸ���֮�ȣ�3:4,�����ȷ�Ĵ�ѡB��
�����Ѷȣ���
4��ѡ���� ����������Һ������������ͭ����������Ϊ��ȥ���ʣ��ᴿ����������Ӧ�ü���������������
A���
B��þ��
C������
D������
�ο��𰸣�C
����������ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��A��п�Ľ�����ǿ������ͭ�ģ����п���û�������ͭ���ò�������������A����ȷ��B��þ�Ľ�����ǿ������ͭ�ģ����þ���û�������ͭ���ò�������������B����ȷ��C�����ܺ�����ͭ��Ӧ��������������ͭ������������Ӧ����������������˿��Դﵽ���ӵ�Ŀ�ģ�C��ȷ��D�����Ľ�����ǿ������ͭ�ģ���������û�������ͭ���ò�������������D����ȷ����ѡC��
�����Ѷȣ���
5��ѡ���� ���й��������仯�����˵������ȷ����
A��Fe3O4�ǡ��ֺ���ɫ��ĩ���׳ƴ���������
B������ˮ�����ڸ����µķ�Ӧ����ΪFe2O3��H2
C��ȥ��FeCl2��Һ�е�FeCl3���ʿ�������Һ�м���������ۣ�Ȼ�����
D��Fe3����KSCN��Ӧ������ɫ����
�ο��𰸣�C
���������A. Fe3O4�ǡ��ֺ�ɫ���壬�׳ƴ�����������? B������ˮ�����ڸ����µķ�Ӧ����ΪFe3O4��H2��D.Fe3����KSCN��Ӧ������ɫ��Һ�����ԣ�ABD����
�����Ѷȣ�һ��