微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (6分)现有一种铜和铁的混合物样品。为测定该样品中铁的含量,某学生取10.0 g此样品置于烧瓶中,将80.0 mL稀硫酸分四次加入烧瓶并做相关记录。
有关数据记录如下表:
加硫酸的序号
| 加入硫酸的体积/mL
| 剩余固体的质量/g
|
1
| 20.0
| 7.20
|
2
| 20.0
| 4.40
|
3
| 20.0
| 2.00
|
4
| 20.0
| 2.00
|
试计算:
(1)此样品中铁的质量分数。
(2)所用硫酸溶液溶质的物质的量浓度。
参考答案:(1)80%?(2)2.5mol/L
本题解析:(1)根据表中数据可知,最后剩余铜2 g,则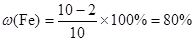
(2) Fe? +? H2SO4? =" Fe" SO4 + H2↑
56g? 1mol
2.8g?c(H2SO4)×0.02L
所用硫酸溶液溶质的物质的量浓度c (H2SO4)=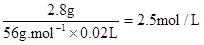
点评:本题主要考查学生的分析能力,很简单基础。
本题难度:一般
2、实验题 (10分)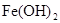 由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用
由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用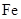 ,
,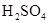 (稀),NaOH溶液可在还原性气氛中制取
(稀),NaOH溶液可在还原性气氛中制取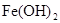 白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.
白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.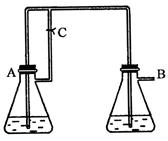
参考答案:铁和稀硫酸 氢氧化钠溶液
①打开弹簧夹C;A中气体由导管进入B,B中有气泡;目的是为了排尽装置和溶液中的氧气,形成还原性气氛;
②过一段时间,关闭弹簧夹C;A中溶液经导管进入B,B中有白色沉淀生成;因为此时A
中压强增大,使得反应生成的FeSO4溶液进入B,而和NaOH反应,生成Fe(OH)2沉淀。
本题解析:要产生还原性的气体,应该用铁和稀硝酸反应生成氢气。即A中的试剂是铁和稀硫酸。利用生成的氢气排尽装置中的空气,从而可以防止氢氧化亚铁被氧化。最后利用氢气产生的越强将硫酸亚铁压入氢氧化钠中进行反应,所以B中的试剂是氢氧化钠溶液。具体的操作是①打开弹簧夹C;A中气体由导管进入B,B中有气泡;目的是为了排尽装置和溶液中的氧气,形成还原性气氛。
②过一段时间,关闭弹簧夹C;A中溶液经导管进入B,B中有白色沉淀生成;因为此时A
中压强增大,使得反应生成的FeSO4溶液进入B,而和NaOH反应,生成Fe(OH)2沉淀。
本题难度:一般
3、选择题 从2 mol ・L-1的氯化铜溶液中取出含Cl―为3.55g的溶液,所取溶液的体积是( )
A.50mL
B.25mL
C.12.5mL
D.0.025mL
参考答案:B
本题解析:略
本题难度:简单
4、填空题 从铝土矿(主要成分是Al2O3,含RO2、Fe2O3等杂质)中提取Al2O3的一种工艺流程如下:
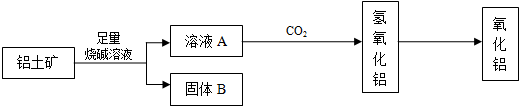
(1)元素R位于周期表中的第三周期,其最高正化合价和负化合价的绝对值相等.RO2的用途有(写出1条即可)______.
(2)铝土矿加入足量烧碱溶液后主要反应的离子方程式为
①______.
②______.
(3)工业上通过电解氧化铝和冰晶石的熔融液来冶炼金属铝.已知电极材料为惰性材料,阳极反应式为______.
(4)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X.已知每转移3mol?e-,有1.5mol化合物X生成,此反应的化学方程式______.
参考答案:(1)最高正化合价和负化合价的绝对值相等,则最外层电子数为4,元素R位于周期表中的第三周期,所以R为硅元素,RO2的是SiO2,其用途有:制作光纤、饰品、建筑材料、石英玻璃、石英坩埚等,
故答案为:制作光纤、饰品、建筑材料、石英玻璃、石英坩埚等;
(2)铝土矿加入足量烧碱溶液,Al2O3、SiO2与氢氧化钠反应,氧化铁不与氢氧化钠反应,
①氧化铝与氢氧化钠反应生成偏铝酸钠和水,反应离子方程式为Al2O3+2OH-=2AlO2-+H2O;?
②二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,离子方程式为SiO2+2OH-=SiO32-+H2O;
故答案为:Al2O3+2OH-=2AlO2-+H2O;SiO2+2OH-=SiO32-+H2O;?
?(3)电解氧化铝和冰晶石的熔融液,生成铝和氧气,氧元素在阳极上被氧化,生成氧气,电极反应式为2O2--4e-=O2↑,
故答案为:2O2--4e-=O2↑;?
(4)根据元素守恒可知X为碳的氧化物,由电子转移守恒,可得在X中C的化合价为3mol1.5mol=2,所以X是CO,所以该反应的化学方程式为Al2O3+N2+3C?高温?.??2AlN+3CO,
故答案为:Al2O3+N2+3C?高温?.??2AlN+3CO.
本题解析:
本题难度:一般
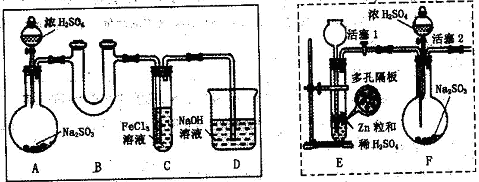
5、实验题 [2012・漳州质检](11分)某研究学习小组为探究Fe3+离子是否能氧化SO2,设计了如下的实验装置(假设实验中所用装置的气密性良好)。
 ?
?
(1)甲同学利用以上实线框内装置制取SO2并进行探究实验。
①装置A中发生反应的化学方程式为?。
②装置B的作用是?。
③反应一段时间后,甲同学取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液观察到有白色沉淀产生。由此他得出结论:Fe3+可氧化SO2。
(2)乙同学认为甲同学的实验不严谨,他用以上虚线框内装置替代装置A,先使装置E内试剂反应一段时间后,关闭活塞1,打开活塞2,又反应片刻后,取装置C中少量溶液,往其中加入酸性KMnO4溶液,观察到KMnO4溶液紫红色褪去。由此他得出结论:Fe3+已被SO2还原成Fe2+。
①该实验制H2时需用浓硫酸配制450mL3mol/L的稀硫酸,配制中所需的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需?。
配制过程中若其它操作无误,但没有洗涤烧杯与玻璃棒,则所配制溶液的浓度会??(填“偏高”、“偏低”或“无影响”)。
②在该实验过程中H2所起得作用是?。
(3)丙同学认为甲、乙的实验均不严谨,为此他沿用乙同学的实验装置及操作,重新实验。待装置F内反应一段时间后,取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液,得出与甲同学相同的结论。请你分析回答:
①甲同学实验不严谨的原因是?。(选填序号)
A.SO2溶解量太小
B.SO2不与Fe3+发生反应
C.H2SO3与BaCl2不反应
D.装置中的空气与SO2进入水中也可生成H2SO4