微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 几种短周期元素的原子半径及主要化合价如下表(?)
元素代号
| L
| M
| X
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.102
| 0.089
| 0.074
|
主要化合价
| +2
| +3
| +6,-2
| +2
| -2
|
下列叙述错误的是
A.R的氧化物对应的水化物可能具有两性? B.X单质在氧气中燃烧不可能生成XO3
C.离子半径大小:r(M3+)>r(T2-)?D.最高价氧化物对应水化物碱性:L(OH)2>M(OH)3
参考答案:C
本题解析:L、M、X、R、T对应的元素分别为: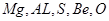 所以
所以
A正确,氢氧化铍具有两性;B正确,S单质燃烧不能生成三氧化硫;C错,离子半径大小关系为:r(T2-)>r(M3+);D正确;镁的金属性比铝强;
本题难度:一般
2、填空题 元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。

(1)阴影部分元素在元素周期表中的位置为________族。
(2)根据元素周期律预测:H3AsO4属于强酸还是弱酸?________。
(3)C和Si元素的氢化物都可以燃烧,但Si元素的氢化物在空气中可以自燃,其原因是_________________________________________。
试写出Si的氢化物完全燃烧的化学方程式:______________________________。
(4)O2与H2的反应是不可逆反应,而S与H2反应有一定限度,请写出Se与H2反应的化学方程式:______________________
(5)试比较S、O、F三种元素的原子半径大小:________(填元素符号)。
参考答案:(1)第ⅤA族 (2)弱酸 (3)SiH4的稳定性小于CH4 SiH4+2O2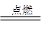 SiO2+2H2O (4)Se+H2
SiO2+2H2O (4)Se+H2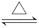 H2Se (5)S>O>F
H2Se (5)S>O>F
本题解析:(1)图中阴影部分为氮族元素,即第ⅤA族。
(2)在周期表中,砷元素的非金属性比磷元素弱,磷酸属于中强酸,故H3AsO4属于弱酸。
(3)甲烷(CH4)燃烧产生二氧化碳和水,硅烷(SiH4)的性质与甲烷相似,它在空气中燃烧的产物应该是水和硅的氧化物,即:SiH4+2O2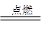 SiO2+2H2O。
SiO2+2H2O。
(4)同主族元素从上到下非金属性逐渐减弱,“S与H2反应有一定限度”属于可逆反应,故Se与H2反应也应该是可逆反应,反应的化学方程式为:Se+H2 H2Se。
H2Se。
(5)S与O同主族,原子序数S>O,故原子半径S>O;O与F同周期,原子序数O<F,故原子半径O>F,所以原子半径:S>O>F。
本题难度:一般
3、推断题 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。
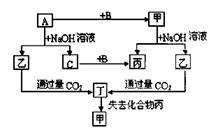
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A ?B?丁?。
(2)元素A在周期表中的位置是?,写出甲的一种用 途?。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式?。
乙与过量CO?2反应的离子方程式?。
参考答案:
(1)Si(2分)? O2(2分)? H2SiO3或H4SiO4(2分)
(2)第三周期第ⅣA族(2分)?是玻璃、光导纤维等(2分)
(3) ①Si+2NaOH+H2O=Na2SiO3+2H2↑(2分)
② SiO32―+2CO?2+2H2O=H2SiO3↓+2HCO3―(2分)
本题解析:根据题意可知A:SiB:O2、C:H2、甲:SiO2、乙:Na2SiO3、丙:H2O、丁:H2SiO3。
(1)突破口:C为密度最小的气体,知C是H2;甲为非电解质,不能是Al2O3,只能是SiO2;则A为Si、B为O2、 乙是Na2SiO3,通CO?2生成丁,丁为H2SiO3。丁失去丙生成甲,丙为H2O。
(2)A为Si,在周期表的第三周期第ⅣA族;用途是做玻璃、光导
本题难度:一般
4、填空题 (7分)按要求填空:
(1)某阴离子核外18电子,带两个单位负电荷,其离子结构示意图?。
(2)含6个质子、8个中子的原子符号为???,它与16O形成3原子分子甲,4.6克甲的物质的量是???mol,甲分子中相邻原子间以??键结合(填“离子键”或“共价键”)。
(3)铁原子核外有4个电子层,在周期表第8列,它在元素周期表的第?周期?族。
(4)盛放碱液的试剂瓶不能用玻璃塞,是为了防止发生?
反应(以NaOH为例用化学方程式表示),避免瓶塞与瓶口粘在一起
参考答案:(1) S2-?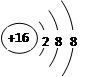 ?(2)(1+1+1分)?146C,? 0.1,共价键?
?(2)(1+1+1分)?146C,? 0.1,共价键?
(3)(1分)四,第Ⅷ
(4)(2分)SiO2 + 2NaOH? =?Na2 CO3+ H2O
本题解析:(1)离子结构示意图为

(2)含6个质子、8个中子的原子符号为146C,甲的物质的量0.1mol,甲分子中相邻原子间以共价键结合
(3)铁在元素周期表的第四周期第Ⅷ族
(4)为了防止发生SiO2 + 2NaOH = Na2 CO3+ H2O
本题难度:一般
5、填空题 (10分)短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D与B属于同一族元素。
(1)元素:A为________,D的质子数和中子数相等,D的原子组成符号为:_________,
它的最高价氧化物对应的水化物为:________。
(2)用电子式表示A、B两元素形成AB2的过程_____________________________
用电子式表示C、D两元素形成化学键的过程_______________________________
参考答案:(1)C 3216S H2SO4
(2)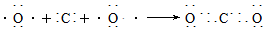

本题解析:两元素的单质反应,生成一种淡黄色的固体E,所以E是过氧化钠,则B是氧元素,C是钠元素。D与B属于同一族元素,因此D是S元素。又因为A的原子序数最小,且A原子的最外层上有4个电子,所以A是碳元素。
(1)A为C,D的质子数和中子数相等,所以D的原子组成符号为S。S元素的最高价是+6价,所以其最高价氧化物的水化物的化学式是H2SO4。
(1)CO2是含有极性键的共价化合物,所以用电子式表示其形成过程是
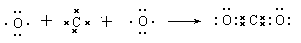 。硫化钠是含有离子间的离子化合物,其形成过程表示位
。硫化钠是含有离子间的离子化合物,其形成过程表示位 。
。
点评:本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。
本题难度:一般