|
���л�ѧ֪ʶ����ɡ����ʵķ��롢�ᴿ������Ԥ�⣨2017�����°棩(��)
2017-07-18 02:01:05
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���г�ȥ���ʵķ�����ȷ����
�� ��ȥ��������������ϩ��ͨ�����Ը��������Һ��ϴ����
�ڳ�ȥ��������������������ñ���̼������Һϴ�ӣ���Һ���������
�� ��ȥCO2��������CO���ڿ����е�ȼ��
�ܳ�ȥ�Ҵ��������������������ʯ�ң�����
A���٢�
B���ڢ�
C���ۢ�
D���ڢ�
�ο��𰸣�B
����������� ������ȥ��������������ϩ��ͨ�����Ը��������Һ��ȥ��ϩ��ͬʱ�������µ����ʶ�����̼���壬��ȷ����Ϊͨ����ˮ���۴� CO2��������CO�ڿ������ܵ�ȼ����ȷ�ķ���Ϊͨ�����ȵ�����ͭ��
�����Ѷȣ�һ��
2��ʵ���� K3[Fe(C2O4)3]��3H2O [���������������ؾ���]������ˮ���������Ҵ�������Ϊ�л���Ӧ�Ĵ�����ʵ���ҿ��÷���м������Ϊԭ���Ʊ������ⶨ��Ʒ�Ĵ��ȡ���ط�Ӧ�Ļ�ѧ����ʽΪ��Fe + H2SO4 ��FeSO4 + H2��? FeSO4��H2C2O4��2H2O��FeC2O4��2H2O����H2SO4
2FeC2O4��2H2O��H2O2��H2C2O4��3K2C2O4��2K3[Fe(C2O4)3]��6H2O
�ش��������⣺
��1��ʹ�÷���мǰ������������1.0mol.L-1Na2CO3��Һ�н���������,��Ŀ����?��Ȼ��ʹ��?����д�������ƣ����벢ϴ����м��
��2��������K3[Fe(C2O4)3]��3H2O�����ͨ������ͼ��ʾװ��ͨ����ѹ������ĸҺ���롣���й��ڼ�ѹ���˵IJ�����ȷ����?��
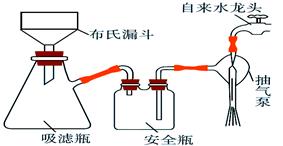
A��ѡ��Ȳ���©���ھ���С���ܽ�ȫ��С��ס����ֽ
B��������ֽ��ֱ����������ת����Һ�ͳ������ٴ�ˮ��ͷ����
C��ϴ�Ӿ���ʱ���ȹر�ˮ��ͷ��������ˮ������ϴ���ٴ�ˮ��ͷ����
D���������ʱ��Ӧ�ȶϿ������ú�����ƿ֮�����Ƥ�ܣ��Է�����
| ��3��ʹ�ø�����ط���һ��������ԭ��Ӧ�ζ��������Բⶨ���ò�Ʒ�Ĵ��ȡ���������Ũ��Ϊ0.03000 mol��L-1KMnO4����Һ240mL��Ӧȷ��ȡ?g KMnO4(������λ��Ч���֣���֪M KMnO4��158.0g.mol-1)�����Ƹñ���Һʱ������������������ƽ��ҩ�ס��ձ����������⣬��ȱ�ٵIJ���������?�����ƹ����У����ӿ̶��߶�������������ҺŨ��?���ƫ����ƫС������Ӱ�족����
��4��ijͬѧ��ȡ2.000g��Ʒ����Ԥ���������Ƴ�100mL��Һ����ȡ25.00mL��Һ����ƿ�У�ʹ��0.03000 mol��L-1KMnO4����Һ�ζ������ı���Һ10.00mL��
��ʵ�ʽ��еζ�ʱ������ʹ���ữ��KMnO4����Һ��д���õζ���Ӧ�����ӷ���ʽ?��
���жϵ���ζ��յ��������?��
�۸ò�Ʒ�Ĵ���Ϊ?����������λ��Ч���֣���
�ο��𰸣���1����ȥ��м��������ۣ�1�֣�?��������1�֣�
��2��AD��2�֣�?��3��1.185��2�֣�? 250mL����ƿ����ͷ�ιܣ�2�֣�?ƫ��1�֣�
��4����2MnO4-? +? 5C2O42-? + 16H+? = 2Mn2+? + 10CO2�� + 8H2O? (2��)
�ڼ������һ��KMnO4����Һ����Һ��dz��ɫ����30s�ڲ��仯��1�֣�?��24.55?��2�֣�
�����������1��̼������ǿ�������Σ���Һ�Լ��ԣ�����ʹ�÷���мǰ������������1.0mol.L-1Na2CO3��Һ�н��������ӵ�Ŀ���dz�ȥ��м��������ۣ��������ǽ�����������ˮ�����Կ���ʹ�����������벢ϴ����м��
��2��A��ѡ��Ȳ���©���ھ���С���ܽ�ȫ��С��ס����ֽ����ֽ��ʱ����ֽ��Ե��©��������϶��ʹ�����ٶ����������鲻�ɣ���ֽСʱ����ֽ���ܸ�ס���пף����ܹ��ˣ���A��ȷ��B��������ֽ���ò�����������ת����Һ�ͳ������ٴ�ˮ��ͷ���ˣ���B����C��ϴ�Ӿ���ʱ���ȹر�ˮ��ͷ��������ˮ������ϴ������ˮ��ͷ����ϴ��Һ������ȫ�����壬��C����D���������ʱ��Ӧ�ȶϿ������ú�����ƿ֮�����Ƥ�ܣ��Է���������D��ȷ����ѡAD��
��3������û��240ml����ƿ������Ӧ������250ml���������Һ������Ҫ������ص�������0.03000 mol��L-1��0.25L��158g/mol��1.185g�����Ƹñ���Һʱ������������������ƽ��ҩ�ס��ձ����������⣬��ȱ�ٵIJ���������250mL����ƿ����ͷ�ιܣ����ƹ����У����ӿ̶��߶�����������ƿ����Һ�����ƫ�٣����������ҺŨ��ƫ��
��4���ٷ�Ӧ��̼Ԫ�صĻ��ϼ۴�+3�����ߵ�+4��ʧȥ1�����ӣ���MnԪ�صĻ��ϼ۴�+7�۽��͵�+2�۵õ�5�����ӣ���˸��ݵ��ӵ�ʧ�غ��֪�������뻹ԭ�������ʵ���֮����2:5�������ԭ���غ��֪����ƽ��ķ���ʽΪ5C2O42����2MnO4����16H��=10CO2��2Mn2����8H2O��
���������Ը��������Һ���Ϻ�ɫ�������жϵ���ζ��յ�������Ǽ������һ��KMnO4����Һ����Һ��dz��ɫ����30s�ڲ��仯��
�۸��ݷ���ʽ��֪���μӷ�Ӧ�IJ���������ʵ�����0.03000 mol��L-1��0.01L�� ��0.0007500mol������2.000g��Ʒ��K3[Fe(C2O4)3]��3H2O��������0.0007500mol�� ��0.0007500mol������2.000g��Ʒ��K3[Fe(C2O4)3]��3H2O��������0.0007500mol��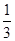 ��491/mol�� ��491/mol��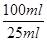 ��0.491g�����Դ���Ϊ ��0.491g�����Դ���Ϊ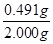 ��100%��24.55%�� ��100%��24.55%��
�����Ѷȣ�����
3������� (18��)Ϊ�˳�ȥKCl��Һ��������MgCl2��MgSO4����ϡ���ᡢNa2CO3��Ba(NO3)2��K2CO3��Ba(OH)2��Һ�У�ѡ��A��B��C 3���Լ�����ͼ�е�ʵ�鲽����в�����

(1)3���Լ��Ļ�ѧʽ��A____?____��B____?____��C____?____��
(2)�ӹ���A��ԭ����________?____��
�йط�Ӧ�Ļ�ѧ����ʽΪ__________________________? _________________________
(3)�ӹ���B��ԭ����______?______?��
�йط�Ӧ�Ļ�ѧ����ʽΪ?
�ο��𰸣���18�֣�(1)Ba(OH)2��K2CO3��ϡHCl
(2)Ϊ�˳���Mg2����SO42-?MgCl2��Ba(OH)2===BaCl2��Mg(OH)2����
MgSO4��Ba(OH)2===BaSO4����Mg(OH)2��
(3)Ϊ�˳���������Ba2����Ba(OH)2��K2CO3===2KOH��BaCO3����
BaCl2��K2CO3===BaCO3����2KCl
���������Mg2�������ù�����OH����ȥ��SO42�������ù�����Ba2����ȥ��������Ҫ���Լ����������������������������������ù�����̼��س�ȥ�����������������ữ���ɡ�����A������������B��̼��أ�C�����ᡣ
�������������л��е����ʳ�ȥ����ô�������ᴿ���������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��
�����Ѷȣ�һ��
4��ѡ���� Ϊ�˳�ȥ����ؾ���������������ƺ�����þ���Ƚ��������Һ��Ȼ���Ⱥ����KOH��K2CO3��Ba��NO3��2���Լ������Թ��ˡ��������ᾧ�Ȳ������Ƴɴ���������ؾ��壬������Լ���˳����ȷ���ǣ�������
A��K2CO3--Ba��NO3��2--KOH--HNO3
B��Ba��NO3��2--KOH--HNO3--K2CO3
C��KOH--K2CO3--Ba��NO3��2--HNO3
D��Ba��NO3��2--KOH--K2CO3--HNO3
�ο��𰸣�Ϊ�˳�ȥ����ؾ���������������ƺ�����þ���Ƚ��������Һ��Ӧ�ȼ���Ba��NO3��2������BaSO4����ȥSO42-��Ȼ����������KOH������Mg��OH��2����ȥMg2+���ټ��������K2CO3������CaCO3��BaCO3��������ȥCa2+��Ba2+��������HNO3��ȥK2CO3��KOH��ע�ⲻ���ȼ�K2CO3�������ܳ�ȥ������Ba2+��
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� ����������Һ�������ͺ��Ȼ�����Һ����39%���Ҵ���Һ�����Ȼ��ƺ͵������ˮ��Һ���������ϸ����Һ����ȷ����������
[? ]
A����Һ����ȡ������?
B����ȡ������Һ
C����Һ��������ȡ?
D��������ȡ����Һ
�ο��𰸣�C
���������
�����Ѷȣ���
|