��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��11�֣���Ч��������������Դ�Ϳ�������Դ���ܵ����������ӡ�
��1�����øĽ�������ɵİ취���������͵�ȼ�����ܡ����磬�������м����Ҵ�����������Ǧ���͡����Ҵ��ķ���ʽΪC2H6O���Ը���C��H��O�ɼ����ص㣬д��C2H6O���п��ܵĽṹʽ��ṹ��ʽ��������������������������?��
��2����Ȼ������Ҫ�ijɷ��Ǽ��飬��ȼ�ղ���������ֵ�ߡ��ܵ����ͷ��㣬����Ϊ�ҹ������������ص�֮һ����˵�������������������������ƽ��ṹ��������?��(��д���)
����һ��ȡ���ﲻ����ͬ���칹��?�������������������ȡ���ﲻ����ͬ���칹��
��������ȡ���ﲻ����ͬ���칹��?��������ȡ���ﲻ����ͬ���칹��
��3������������δ����������Դ��1980���ҹ��״��Ƴ�һ��ȼ����������Ա12�ˣ���50km/h ���ٶ���ʻ��40km��Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������мȿ����־��õ����ⷽ����?��������������?����д��ţ�
���ٶ���ʻ��40km��Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������мȿ����־��õ����ⷽ����?��������������?����д��ţ�
�ٵ��ˮ?��������п��ϡ���ᷴӦ?�����۹�⺣ˮ
��Σ��Ƶô���������Ҫ�����������?����д�����е�һ����
 ��4��������������ȼ������ˮ���Ȼ�ѧ����ʽ
��4��������������ȼ������ˮ���Ȼ�ѧ����ʽ
 2H2��g��+? O2(g) ="=" 2H2O(g)?��H��a kJ/mol
2H2��g��+? O2(g) ="=" 2H2O(g)?��H��a kJ/mol
 2H2��g��+? O2(g) ==2H2O(l)?��H��b kJ/mol
2H2��g��+? O2(g) ==2H2O(l)?��H��b kJ/mol
��ش��������⣺����ʾ����b���ʾb�ľ���ֵ��
 ����2 molH2��ȫȼ������ˮ��������ų����������������������������������b��kJ
����2 molH2��ȫȼ������ˮ��������ų����������������������������������b��kJ
�� ����֪��1mol�����еĻ�ѧ��Ҫ����436 kJ��������1mol�����еĻ�ѧ��Ҫ
����֪��1mol�����еĻ�ѧ��Ҫ����436 kJ��������1mol�����еĻ�ѧ��Ҫ ����496kJ������ˮ������1molH��O���γ�ʱ�ų�����463kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��
����496kJ������ˮ������1molH��O���γ�ʱ�ų�����463kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��
? ?
?
�ο��𰸣�
��1��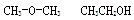
��2����
��3����?���������������
��4���٣�? ��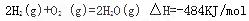
�����������
�����Ѷȣ���
2��ѡ���� �����й������¼���������ȷ����
A���ڽ����·�������Σ�����������ˮ������ѧ��Ӧ�ų�������������ʹ��ѩ�ڻ�
B���ҹ������ƹ�ʹ�ó����Ҵ����ͣ��Ҵ�������һ�����͵Ļ�������ڿ�������Դ
C�����캽�շ��ġ�������ά���͡�������Ҫ�ɷ���̼���衢�մɺ�̼��ά���϶��ɣ�����һ���������ǽ�������
D������ɫӫ�⵰���ʡ����ɰ�����Ӿ۶��ɵĸ߷��ӻ�����
�ο��𰸣�C
���������A �����ڽ����·�������Σ��������۵�ȴ�ˮ���۵�ͣ��ڽϵ��¶ȿ�ʹ��ѩ�ڻ�����һ�������仯
B �����Ҵ����Ͳ���һ�����͵Ļ������һ�����͵����ȼ��
C ��ȷ��̼���衢�մɺ�̼��ά���϶��ɵIJ������������ǽ�������
D �����ɰ��������۶��ɵĸ߷��ӻ�������ǼӾۡ�
�����Ѷȣ�һ��
3��ѡ���� �������ڹ����ι�ҵ��Ʒ���ǣ�������
A��ˮ��
B�������
C��ɳ��
D���մ�
�ο��𰸣�AD
���������
�����Ѷȣ���
4��ѡ���� ����Ԫ�صĵ����ڹ�ҵ���õ�ⷨ��������
A����
B����
C����
D����
�ο��𰸣�B
���������A����������Ҫ��Դ�ǿ��������������仯��A����ȷ��B����ҵ��ͨ�����ʳ��ˮ�õ�������B��ȷ��C����������Ҫ�Ӻ�ˮ�л�ã���Ҫ�Ƿ���������ԭ��Ӧ������Ҫͨ����ⷨ��C����ȷ��D��ͬ�����ʵ���Ҫ�Ӻ�ˮ�л�ã���Ҫ�Ƿ���������ԭ��Ӧ������Ҫͨ����ⷨ��D����ȷ����ѡB��
�����Ѷȣ���
5��ѡ���� ����ѧ����ѡ��2����ѧ�뼼������15�֣�̼�����;�㷺���������մɡ�ҩ�������Ҳ�dz��õ�����ӵ�ص�ԭ�ϡ���ҵ����﮻�ʯ��Li2O��Al2O3��4SiO2��������Ca��MgԪ�أ�Ϊԭ������̼��ﮡ��䲿�ֹ����������£�?
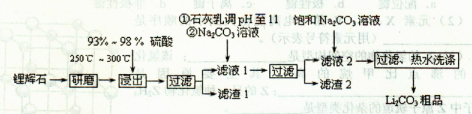
��֪����Li2O��Al2O3��4SiO2+H2SO4��Ũ��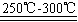 Li2SO4+Al2O3��H2O��
Li2SO4+Al2O3��H2O��
��ijЩ���ʵ��ܽ�ȣ�S�����±���ʾ��
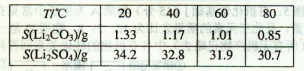
��1��������1�з����Al2O3�IJ�����������ͼ��ʾ�����ű�ʾ������Լ��������ʾ���õ������ʡ�
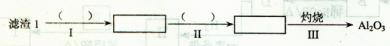
����I�з�Ӧ�����ӷ���ʽ��?�������Ӧͨ��һ�������Լ�Ϊ?������II��Ӧ��֮����Ҫ�IJ�����?��
��2����֪����2����Ҫ�ɷ���Mg��OH��2��CaCO3������Һl�м���ʯ����������ǣ������ӷ���ʽ��ʾ��?��
��3������Һ2�м��뱥��Na2CO3��Һ�����˺��á���ˮϴ�ӡ���ԭ����?��
��4����ҵ�ϣ���Li2CO3�ֲ�Ʒ�Ʊ��ɸߴ�Li2CO3�IJ��ֹ������£�
a����Li2CO3�������������۵�����Һ��LiOH��Һ������Һ������������ѡ����Ĥ�������ö��Ե缫��⡣
b��������LiOH��Һ�м���� ��NH4HCO3��Һ�����ˡ���ɵøߴ�Li2CO3��
��a�У������ĵ缫��Ӧʽ��?��
��b�У�����Li2CO3��Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���1��Al2O3 +6H+ = 2Al3++3H2O��2�֣� NH3 ��2�֣� ���ˣ�2�֣�
��2��Ca(OH)2 + 2H+ = Ca2+ + 2H2O��1.5�֣�Ca(OH)2(s) + Mg2+ Mg(OH)2(s) +Ca2+��1.5�֣�
Mg(OH)2(s) +Ca2+��1.5�֣�
��3�� Li2CO3���ܽ�����¶����߶���С����ˮϴ�ӿɼ���Li2CO3����ʧ��2�֣�
��4���� 2Cl���D2e����Cl2����2�֣��� 2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��2�֣�
������������⿼��Ԫ�ػ���������ʼ���ѧ�뼼���й�֪ʶ����1�����ὫAl2O3��Һ�⣬��ͨ�백��ת��ΪAl(OH)3���������˺����յõ�Al2O3������I�з�Ӧ�����ӷ���ʽ��Al2O3 +6H+ = 2Al3++3H2O��ͨ�������������NH3������II��Ӧ��֮����Ҫ�IJ����ǹ��ˡ���2������Һl�м���ʯ����������ǵ�����Һ��pHֵ����Mg2+ת��Ϊ���ܵ�Mg(OH)2��������Ӧ�����ӷ���ʽΪCa(OH)2 + 2H+ = Ca2+ + 2H2O��Ca(OH)2(s) + Mg2+ Mg(OH)2(s) +Ca2+����3���ӱ������ݿ�֪��Li2CO3���ܽ�����¶����߶���С��������ˮϴ���ܼ���Li2CO3����ʧ����֤���ߵIJ��ʡ���4����Li2CO3�������ᣬ�õ�LiCl��Һ�����ʱ������Cl-ʧ���ӱ����������缫��ӦʽΪ2Cl���D2e����Cl2����Li+ͨ����Ĥ�������������õ�LiOH��Һ���ڵ���õ�LiOH��Һ������NH4HCO3����LiOHת��ΪLi2CO3����Ӧ�Ļ�ѧ����ʽ��2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��
Mg(OH)2(s) +Ca2+����3���ӱ������ݿ�֪��Li2CO3���ܽ�����¶����߶���С��������ˮϴ���ܼ���Li2CO3����ʧ����֤���ߵIJ��ʡ���4����Li2CO3�������ᣬ�õ�LiCl��Һ�����ʱ������Cl-ʧ���ӱ����������缫��ӦʽΪ2Cl���D2e����Cl2����Li+ͨ����Ĥ�������������õ�LiOH��Һ���ڵ���õ�LiOH��Һ������NH4HCO3����LiOHת��ΪLi2CO3����Ӧ�Ļ�ѧ����ʽ��2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��
�����Ѷȣ���