��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������߲������մ���Ʒ���ǣ�������
A��������
B��ɰ��
C��������
D��������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� ����������SnSO4�������ڶ�����ҵ��ijС�����SnSO4�Ʊ�·��Ϊ��
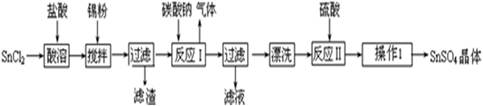
�������ϣ�
�����������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�������
��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����
��1����ԭ�ӵĺ˵����Ϊ50����̼Ԫ��ͬ����A�壬��λ�����ڱ��ĵ�?���ڣ�1�֣�
��2���������� ?���ˡ�ϴ�ӵȣ�2�֣�
��3���ܽ�SnCl2��ĩ���Ũ���ᣬԭ����??
��4������Sn�۵��������������ٵ�����ҺpH?��?
��5����Ӧ��õ�������SnO���õ��ó��������ӷ�Ӧ����ʽ��?
��6�����������£�SnSO4��˫��ˮȥ��Ӧ�����ӷ���ʽ��?
��7����С��ͨ�����з����ⶨ�������۵Ĵ��ȣ����ʲ����뷴Ӧ����
�ٽ��������������У������ķ�ӦΪ��Sn+2HCl�TSnCl2+H2����
�ڼ��������FeCl3��
������֪Ũ�ȵ�K2Cr2O7�ζ������ɵ�Fe2+���ټ������۵Ĵ��ȣ�����ƽ����ʽ��
FeCl2 +?K2Cr2O7 +?HCl = ?FeCl3 + ?KCl + ?CrCl2+?
�ο��𰸣�32.��16�֣���1���������ڣ�1�֣���?��2������Ũ������ȴ�ᾧ��2�֣���
��3��?����Sn2+ ��ˮ�⣨2�֣���?��4����ֹSn2+ ��������2�֣���
��5��SnCl2 + Na2CO3=" SnO��+" CO2��+ 2NaCl��3�֣�δд���͡����Ź���1�֣�δ��ƽ��1�֣�
��6��Sn2+ + H2O2 +2H+ = Sn4 + + 2H2O ��3�֣�δ��ƽ��1�֣�
��7���� 6? 1? 14? 6? 2? 2? 7 H2O��3�֣���ѧʽH2O��1�֣�ϵ��ȫ��2�֣�
���������
�������: �⣺��1����Ԫ����̼Ԫ������ͬһ���壬���ڢ�A�壬ԭ�Ӻ˵����Ϊ50����50-2-8-8-18=14����Sn���ڵ������ڡ�
��2��������ͼ��֪���������Ǵ���Һ�еõ����ᾧˮ�ľ��壬ֻ�ܲ�ȡ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���
��3������Ϣ��֪��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����������ˮ��ƽ��SnCl2+H2O Sn(OH)Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⡣
Sn(OH)Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⡣
��4������Ϣ��֪��Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+��������?
��5����Ӧ��õ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ��ͬʱ�������壬������Ϊ������̼����Ӧ����ʽΪ��SnCl2 + Na2CO3=" SnO��+" CO2��+ 2NaCl��
��6�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ�����ӷ���ʽΪ��Sn2++H2O2+2H+�TSn4++2H2O��
��7����Ӧ������HԪ�أ������������������������ΪH2O�����Ը��ݵ��ǵ����غ���ƽ�ķ���ʽΪ��6FeCl2+K2Cr2O7+14HCl�T6FeCl3+2KCl+2CrCl3+7H2O
�����Ѷȣ�����
3������� ú����Ҫ����Դ��Ҳ������������Ʒ����Ҫԭ�ϡ�������ѧ֪ʶ������������⣺
��1��ú��ת����������ú������������Һ��������ú��Һ�������ַ�Ϊ?��?��
��2����úȼ��ǰ���ú������������ú��ij����������ԭ������ͼ��ʾ��
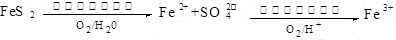 ?
?
������������Ϊ�������������ü����ĵ�һ����Ӧ�����ӷ���ʽΪ??���ڶ�����Ӧ�����ӷ���ʽΪ??��
��3����ҵú����õ��IJ�Ʒ�н�̿��??��
��4����ҵ����Ҫ���ð��������������ᣬ��ͼ�ǰ��������백������������������ȵĹ�ϵ������ֱ�߱�ʾ��Ӧ������ֵ�����߱�ʾ����ʵ����������������ʴﵽ100���������Ϧã�n(O2)��n(NH3)����??��ʵ������Ҫ����ֵά����1.7��2.2֮�䣬 ԭ����?��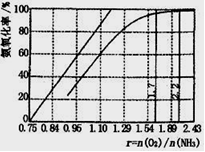
�ο��𰸣�����8�֣���1��ֱ��Һ�����������Һ��������ȫ�Ը�1�֣�
��2��2FeS2��7O2��2H2O 4H+��2Fe2+��4SO42-��2�֣� 4Fe2+��O2��4H+
4H+��2Fe2+��4SO42-��2�֣� 4Fe2+��O2��4H+ 4Fe3+��2H2O��2�֣�
4Fe3+��2H2O��2�֣�
��3����¯ú�����ְ�ˮ��ú���ͣ�ȫ�Ը�1�֣�
��4��1.25��1�֣���? O2̫�ٲ�����NH3��ת������ֵΪ2.2ʱNH3�������ѽ�100%��1�֣�
�����������1��ú��Һ����Ϊֱ��Һ���ͼ��Һ��������
��2����һ����Ӧ�з�Ӧ����FeS2��O2��H2O����������Fe2+��SO42-����Ӧ��SԪ�صĻ��ϼ۴ӣ�1�����ߵ���6�ۣ�ʧȥ7�����ӡ���Ԫ�صĻ��ϼ۴�0�۽��͵���2�ۣ����Ը��ݻ��ϼ�������������Լ�ԭ���غ��֪���÷�Ӧ�����ӷ���ʽΪ2FeS2��7O2��2H2O 4H+��2Fe2+��4SO42-��Fe2+���л�ԭ�ԣ��ɱ���������ΪFe3+��ͬ�����ݻ��ϼ�������������Լ�ԭ���غ��֪���÷�Ӧ�����ӷ���ʽΪ4Fe2+��O2��4H+
4H+��2Fe2+��4SO42-��Fe2+���л�ԭ�ԣ��ɱ���������ΪFe3+��ͬ�����ݻ��ϼ�������������Լ�ԭ���غ��֪���÷�Ӧ�����ӷ���ʽΪ4Fe2+��O2��4H+ 4Fe3+��2H2O��
4Fe3+��2H2O��
��3����ҵú����õ��IJ�Ʒ�н�̿����¯ú�����ְ�ˮ��ú���͡�
��4�����ݰ������Ļ�ѧ����ʽ4NH3+5O2 4NO+6H2O��֪���������ʴﵽ100%�������Ϧ�{n��O2��:n��NH3��}��5:4��1.25�������ڷ�Ӧ��O2Ũ��̫�ٲ�����NH3��ת�������ڦ�{n��O2��/n��NH3��ֵΪ2.2ʱNH3�������ѽ�100%������ʵ������Ҫ����ֵά����1.7��2.2֮�䡣
4NO+6H2O��֪���������ʴﵽ100%�������Ϧ�{n��O2��:n��NH3��}��5:4��1.25�������ڷ�Ӧ��O2Ũ��̫�ٲ�����NH3��ת�������ڦ�{n��O2��/n��NH3��ֵΪ2.2ʱNH3�������ѽ�100%������ʵ������Ҫ����ֵά����1.7��2.2֮�䡣
�����Ѷȣ�һ��
4��ѡ���� ���������У������й����ε��ǣ�������
A������
B�����
C����оƬ
D����ͨˮ��
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ����˵����ȷ����
A�������ʡ���ά�����ǡ�����ϩ�����۶��Ǹ߷��ӻ�����
B�������Ҵ����ͣ�����������һ���������Ҵ������������Խ��ͻ�������β�����к������ŷ�
C��ʹ��̫������ˮ�������������á��������Ҵ����漰���������ܵ�����
D��ʯ�͡�ú����Ȼ������ȼ����ֲ���Ͷ����ڻ�ʯȼ��
�ο��𰸣�B
���������A�����Dz��Ǹ߷��ӻ�����ų�
B����ȷ
C��̫������ˮ���ǽ�̫����ֱ��ת��Ϊ���ܣ����漰���������ܵ����ã��ų�
D��ֲ���Ͳ����ڻ�ʯȼ��
�ʴ�ΪB
�����Ѷȣ�һ��