��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ӵ��ʷ����⣬��������в��ܷ�ӳ�����ǵ�������ǿ����ͬ���ǣ�?��
A�����ʸ�±����֮����û����
B��������϶��γɵ�±��������ɫ�仯���
C����������Ӧ�����
D����ˮ��Ӧ�����
�ο��𰸣�B
������������ʵ�������ǿ������Ϊ���ʵĵõ�������������±��֮����û�����������Ӧ�����ף���ˮ��Ӧ��������жϣ����ܴ����������磺��ɫ��״̬���ܶȡ��ܽ�ȵ����жϣ�Ҳ���ܴ��仯�������ɫ���жϡ�
�����Ѷȣ���
2������� ��10�֣����ֹ�������ˮ��ɱ��������Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��Ư���dz��õ���������
��1����ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]��ȡƯ�ۣ���ѧ��Ӧ����ʽΪ?��
��2��ʵ���ҳ������̿���Ҫ�ɷ�ΪMnO2�� ��Ũ���ᷴӦ��Cl2���仯ѧ����ʽΪMnO2+4HCl(Ũ)
��Ũ���ᷴӦ��Cl2���仯ѧ����ʽΪMnO2+4HCl(Ũ)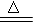 ?MnCl2+Cl2 ��+ 2H2O�����У�����������?���ѧʽ�����������뻹ԭ�������ʵ���֮��Ϊ??�������ɵ�Cl2�ڱ�״���µ����Ϊ672 ml ,��ת�Ƶ���??mol?��
?MnCl2+Cl2 ��+ 2H2O�����У�����������?���ѧʽ�����������뻹ԭ�������ʵ���֮��Ϊ??�������ɵ�Cl2�ڱ�״���µ����Ϊ672 ml ,��ת�Ƶ���??mol?��
��3������Cl2�Ѽ����ķ�����??��
�ο��𰸣���10�֣�.��1�� 2Ca(OH)2 + 2Cl2 = CaCl2 + Ca(ClO)2 + 2H2O
��2�� Cl2 ??1�U2 ??0.06 ?
��3����ʪ��ĵ���KI��ֽ���ڼ���ƿ�ڣ����������Ѽ���������������Ҳ�ɣ�
�����������
�����Ѷȣ���
3������� ��18�֣�ij��ѧ�о�С��̽���廯����ˮ��Һ��������Ӧ��
��1����С��ͬѧ����ͼ��ʾװ����ȡ���﴿����������

����A��������________��װ��C�е��Լ���________��װ��F��������________��д���Ʊ����������ӷ���ʽ________��
��2����С��ͬѧ��Cl2��FeBr2��Һ�ķ�Ӧ����ʵ��̽����
��ʵ����̡�
��l00mL0. 1mol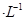 ����Һ����ͨ��100 mLCl2����״��������Һ��dz��ɫ���ɫ������ͨ��Cl2����Һ��ɫ�����Ϊ�ػ�ɫ��
����Һ����ͨ��100 mLCl2����״��������Һ��dz��ɫ���ɫ������ͨ��Cl2����Һ��ɫ�����Ϊ�ػ�ɫ��
��������衿������������ԭ������ǣ�
����1��Cl2�Ƚ�Fe2����������Fe3������Һ���ɫ��Cl2�ٰ�Br��������Br2����Һ��Ϊ�ػ�ɫ��
����2��Cl2�Ƚ�Br����������Br2����Һ���ɫ��Cl2�ٰ�Fe2��������Fe3������Һ��Ϊ�ػ�ɫ��
��ʵ�鷽����
�����ף����ʵ����֤��dz��ɫ���ɫ��ԭ��________��˵��ʵ�����������ͽ��ۣ���
�����ң���ƶԱ�ʵ����֤������˳��

����ʵ��ó�Cl2��Fe3����Br2��������ǿ������˳��Ϊ________�����������������________��
��3��������0.1 molFeBr2����Һ��ͨ��0.1molCl2��ַ�Ӧ��д����Ӧ�����ӷ���ʽ��________ ��
�ο��𰸣���18�֣�
��1����Һ©����1�֣�?����ʳ��ˮ��2�֣���ȥβ���е�������ֹ��Ⱦ������2�֣�
MnO2+4H++2Cl? Mn2++Cl2��+2H2O��2�֣�
Mn2++Cl2��+2H2O��2�֣�
��2����ȡ����������ɫ��Һ���Թ��У������еμ�����KSCN��Һ��������Һ���ɫ��˵������1�ԣ�����������3�֣���ȡ����������ɫ��Һ���Թ��У������еμ�����CCl4������CCl4����ֳȺ�ɫ��˵������2�ԣ�����������3�֣�
��ȡ�����廯����Һ���Թ��У������еμ�������ˮ������CCl4�����ã�2�֣� Cl2 > Br2 >Fe3+��2�֣�
����1��1�֣�
��3��2Fe2++2Br?+2Cl2 = 2Fe3++Br2+4Cl?��3�֣�
�����������1������ʵ��װ��ͼ������A������Ϊ��Һ©����MnO2��Ũ���ᷴӦ��ȡ�������к���HCl��ˮ�֣�����װ��C�е��Լ��DZ���ʳ��ˮ������������HCl���ʣ������ж��������ŷŵ������У�����װ��F�������ǣ���ȥβ���е�������ֹ��Ⱦ������MnO2��Ũ���ᷴӦ����MnCl2��Cl2��H2O�����ӷ���ʽΪ��MnO2+4H++2Cl? Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
��2���ٸ��ݼ�������ʵ�鷽����Ӧ������Һ���Ƿ���Fe3+������ʵ�����������ͽ���Ϊ��ȡ����������ɫ��Һ���Թ��У������еμ�����KSCN��Һ��������Һ���ɫ��˵������1�ԣ������������ݼ�������ʵ�鷽����Ӧ������Һ���Ƿ���Br2������ʵ�����������ͽ���Ϊ��ȡ����������ɫ��Һ���Թ��У������еμ�����CCl4������CCl4����ֳȺ�ɫ��˵������2�ԣ���������
��ʵ������Ϊ��CCl4������ɫ��Ϊ��ɫ��˵��������Br2��Ӧ����Cl2������ʵ�����Ϊ��ȡ�����廯����Һ���Թ��У������еμ�������ˮ������CCl4�����ã������������������Դ�����������������Կɵ���������ǿ������˳��Ϊ��Cl2 > Br2 >Fe3+����ԭ����ǿ������˳��Ϊ��Fe2+ > Br? > Cl?������Cl2��������ԭ��ǿ��Fe2+���ʼ���ٺ�����
��3������0.1 molFeBr2����Һ��ͨ��0.1molCl2��ַ�Ӧ��Cl2������0.1mol Fe2+������Cl2 0.05mol��ʣ���0.05mol Cl2������0.1mol Br?���������ӷ���ʽΪ��2Fe2++2Br?+2Cl2 = 2Fe3++Br2+4Cl?
�����Ѷȣ�һ��
4��ѡ���� ����ʵ��������������ˮ�е�ijЩ�ɷ�(����������)û�й�ϵ����(? )
A����NaHCO3�������������ˮ�У�����ɫ���ݲ���(H��)
B��ʹ��ɫ������ɫ(HCl)
C����FeCl2��Һ�еμ���ˮ���ٵμ�KSCN��Һ�����ֳʺ�ɫ(Cl2)
D���μ�AgNO3��Һ���ɰ�ɫ����(Cl��)
�ο��𰸣�B
�����������ˮ�д���H������NaHCO3��Ӧ����CO2����ˮʹ��ɫ������ɫ����Ϊ��ˮ�д���HClO����������Ϊ��ˮ�д���HCl����ˮ�д��ڵ�Cl2������Fe2���D��Fe3�����ʵμ�KSCN��Һ����Һ�ʺ�ɫ����ˮ�д��ڵ�Cl������AgNO3��Һ���ɰ�ɫ������
�����Ѷȣ���
5������� (6��) ��Ԫ���ж��ֻ��ϼۣ������ǰ���Ԫ�ػ��ϼ��ɵ͵������еĶ������ʣ�NaCl��?��HClO��Ca(ClO)2��KClO3�����������ѡ����ʵĻ�ѧʽ��գ�
��1��������Ԫ�صĻ��ϼ۱仯��������Ӧ���������Ϊ?��
��2���������Ȼ������У������������ʵ�����Ʊ���������?��
��3���������Ȼ������У���ˮ��Һ�������Ժ�Ư���Ե���?��
�ο��𰸣�
��1��Cl2?��2��KClO3
��3��HClO
����� ������
�����Ѷȣ���