微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念。下表给出的是第三周期的七种元素和第四周期的钾元素的电负性的值。下列说法不正确的是

[? ]
A.?钙元素的电负性的取值范围在0.8与1.2之间?
B.?硫化钠的电子式为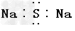 ?
?
C.?硅元素的电负性的取值范围?在1.5与2.1之间
D.?Al与S形成的化学键可能为共价键
2、选择题 关于电负性的叙述不正确的是
[? ]
A.两原子形成共价键时对其共用电子的吸引力大小可用电负性衡量
B.氟原子第一电离能最大,电负性也最大
C.同周期主族元素的电负性数值由左向右逐渐增大
D.分析元素电负性数值可以看出,金属元素的电负性较大,非金属元素的电负性较小
3、填空题 W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X原子核外电子层数等于最外层电子数,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第____周期第____族。W的气态氢化物稳定性比H2O(g)____(填“强”或“弱”)。
(2)Y的原子核外电子排布示意图是____,Y的第一电离能比X的___(填“大”或“小”)。
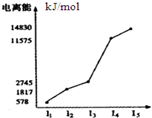
4、选择题 某元素X的逐级电离能如图所示,下列说法正确的是( )
A.X元素显+4价
B.X为非金属
C.X为第五周期元素
D.X与氯反应时最可能生成的阳离子为X3+