微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知ICl与锌和水的反应如下:2ICl+2Zn ═ ZnI2+ZnCl2,ICl+H2O ═ HCl+HIO,下列说法正确的是(?)
A.ZnCl2既是氧化产物又是还原产物
B.ZnI2既是氧化产物又是还原产物
C.在ICl与水反应中,ICl是氧化剂、H2O是还原剂
D.ICl与水反应是氧化还原反应
参考答案:B
本题解析:A、B项:反应中,Zn元素的化合价升高,I元素的化合价降低,则ZnI2既是氧化产物又是还原产物,故A错B正确;
B、反应①中,I元素的化合价降低,则ICl只作氧化剂,故B错误;
C、D项:反应中,没有元素的化合价变化,则不是氧化还原反应,故C、D错误。
故选B。
点评:本题属于信息习题,注意类推的规律及准确判断ICl中I为+1价,Cl为-1价是解答本题的关键,然后利用化合价来分析反应即可。
本题难度:一般
2、填空题 某反应中反应物与生成物有: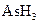 、
、 、
、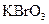 、
、 、
、 、
、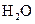 和一种未知物质X。
和一种未知物质X。

 (1)已知
(1)已知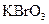 在反应中得到电子,则该反应的还原剂是?。
在反应中得到电子,则该反应的还原剂是?。
 (2)已知0.2mol
(2)已知0.2mol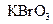 在反应中得到1mol电子生成X,则X的化学式为?。
在反应中得到1mol电子生成X,则X的化学式为?。
 (3)根据上述反应可推知?。
(3)根据上述反应可推知?。
 ? a.氧化性:
? a.氧化性: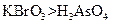 ? b.氧化性:
? b.氧化性: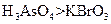
 ? c.还原性:
? c.还原性: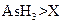 ? d.还原性:
? d.还原性: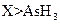
 (4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
 向和数目:
向和数目:
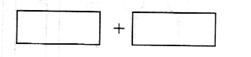
参考答案:
 (1)AsH3
(1)AsH3
 (2)Br2
(2)Br2
 (3)ac
(3)ac
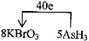
 (4)?
(4)?
本题解析:(1)KBrO3在反应中得到电子,则另外一种化合价变化的元素在反应中失去电子被氧化,所给物质中As元素化合价发生了变化,低价态的AsH3是还原剂。
(2)0.2mol KBrO3得到1mol电子,说明Br元素在反应中降低了5价,所以x的化学式为Br2。
(4)利用氧化还原反应中电子得失相等的规律可配平该方程式为
8KBrO3+5AsH3+4H2SO4===4K2SO4+4Br2+5H3AsO4+4H2O
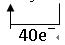

本题难度:一般
3、选择题 下列反应中,通入的气体物质只作为氧化剂的是( )
A.二氧化硫通入氯水中
B.氯气通入氢氧化钠溶液中
C.氯气通入氯化亚铁溶液中
D.氨气通入水中
参考答案:C
本题解析:A中S元素的化合价升高,作还原剂。B中氯气既是氧化剂,又是还原剂。C中氯气得到电子,化合价降低,是氧化剂。D不是氧化还原反应,答案选C。
本题难度:简单
4、选择题 ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
2KClO3+H2C2O4+H2SO4==2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的是
[? ]
A.KClO3在反应中失去电子
B.ClO2是氧化产物
C.1molKClO3参加反应有2mol电子转移
D.H2C2O4在反应中被氧化
参考答案:D
本题解析:
本题难度:简单
5、选择题 某反应体系中的物质有 ,已知Zn是反应物,下列说法错误的是
,已知Zn是反应物,下列说法错误的是
A.反应中氧化剂与还原剂的物质的量之比为14:5
B.反应中还原剂与氧化产物的物质的量之比为1:1
C.若1mol Zn参与反应.则转移的电子数约为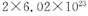
D.若把该反应设计成原电池,则负极的电极反应式为
参考答案:A
本题解析:该反应的方程式为:11Zn + 28HNO3===== 11Zn(NO3)2 + 2NH4NO3 + 2NO + 10H2O;
A错,在该反应中Zn是还原剂,HNO3是氧化剂,其物质的量之比为11:28;
B正确,在该反应中Zn是还原剂,Zn(NO3)2为氧化产物,它们物质的量之比1:1
C正确,若1mol Zn参与反应.则转移的电子数约为: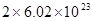
D正确,在原电池中,负极为失去电子的一极,失去电子后元素的化合价升高,其电极反应式为:Zn—2e—=Zn2+
本题难度:一般