��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �Ȼ������ճ����������dz��õĵ�ζƷ���������ʿ���֤���Ȼ�����һ���������Ӽ����ǣ�������
A�����нϸߵ��۵�
B��ˮ��Һ�ܵ���
C������״̬�ܵ���
D��������������ˮ
2��ѡ���� �����й����ʽṹ�ı�����ȷ����
[? ]
A��������ĵ���ʽ?
B����������ķ���ʽSiO2
C��CS2�ĽṹʽS��C��S
D�������ӵĽṹʾ��ͼ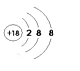
3��ѡ���� ���зǼ��Լ��ҷ����и�ԭ�Ӷ�����8�����ȶ��ṹ����
[? ]
A��CH4
B��CO2
C��BeCl2
D��N2
4������� ��13�֣� ���ֳ���Ԫ�ص����ʻ�ṹ��Ϣ���±����Ը�����Ϣ�ش��й����⡣
Ԫ��
| A
| B
| C
| D
|
����
�ṹ
��Ϣ
| ԭ�Ӻ������������Ӳ㣬�������3��δ�ɶԵĵ���
| ԭ�ӵ�M����1�ԳɶԵ�p����
| ԭ�Ӻ�������Ų�Ϊ[Ar]3d104s1��
��+1��+2���ֳ������ϼ�
| �����ֳ��������������һ����ұ��ҵ���õĻ�ԭ��
|
��д��Bԭ�ӵĵ����Ų�ʽ?��
��AԪ�ص��⻯��ķе��ͬ��������Ԫ���⻯��е�?����ߡ��͡���������__________________________��
��D�����������ĵ���ʽ��?��������D�������ﻹԭ������ķ���ʽΪ���淴Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ___________________���÷�Ӧ��ƽ�ⳣ������ʽK=___________��
����CԪ�ص���������Һ����μ������AԪ�ص��⻯��ˮ��Һ�������ɵ������Ļ�ѧʽΪ________________����Ҫ������������л�ѧ���ijɼ����__________________��
�����з��ӽṹͼ�еġ� ����ʾ�������Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣���
����ʾ�������Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣��� ����ʾ��ԭ�ӣ�С�ڵ㡰
����ʾ��ԭ�ӣ�С�ڵ㡰 ����ʾû���γɹ��ۼ����������ӣ����߱�ʾ���ۼ���
����ʾû���γɹ��ۼ����������ӣ����߱�ʾ���ۼ���
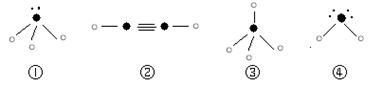
�������Ϸ����У�����ԭ�Ӳ���sp3�ӻ��γɻ�ѧ�����ҿռ乹���ǽ��ε���?����д��ţ����ڢڵķ�������?���Ҽ���?���м���
����֪NH4+��N4H44+�Ŀռ乹�;�Ϊ�����壬NH4+�ĽṹʽΪ sup10(�O��N��,sup10(�OH������ʾ���õ��Ӷ���Nԭ�ӵ������ṩ���� �뻭��N4H44+�Ľṹʽ_____________________��
5��ѡ���� ���з����У����зǼ��Լ��Ļ������ǣ�? ��
A��H2
B��CO2
C��H2O
D��C2H4